
|
Eng |
ศ.ดร. อำพล ไมตรีเวช*, ศ.ดร. ณรงค์ สาริสุต, ภญ. ดวงมณี มณีโรจน์ภักดี, ภญ. วสุ วิฑูรย์สฤษฏ์ศิลป์ และ ภก. โกศล แซ่ติ้ง ภาควิชาเภสัชอุตสาหกรรม คณะเภสัชศาสตร์ มหาวิทยาลัยมหิดล
บทนำ
ระบบนำส่งเป็นศาสตร์ที่อาศัยความรู้จากสหวิชาไว้ด้วยกัน และเป็นแขนงที่ได้รับความสนใจจากทั้งนักวิจัย ในทศวรรษที่ผ่านมาได้มีการศึกษาเทคโนโลยีการนำส่งยาที่หลากหลาย แต่ที่ได้รับความสนใจเป็นอันมากคือ การพัฒนาระบบนำส่งในระดับนาโนเมตร หรือที่เรียกว่า ‘อนุภาคนาโน’ ได้มีการพัฒนาอนุภาคนาโนไปใช้กับทั้งยาที่มีการใช้ในรูปแบบเดิม การนำส่งยาโปรตีน วัคซีน และนิวคลีโอไทด์ เป็นต้น โดยระบบนำส่งที่พัฒนาขึ้นทั้งในรูปอนุภาคนาโน หรือระบบคอลลอยด์อื่นๆ เหล่านี้ จะไปมีผลต่อค่าเภสัชจลนศาสตร์ การกระจาย และการปลดปล่อยในร่างกาย(1)
นอกจากนี้ในปัจจุบันได้มีการประยุกต์ใช้อนุภาคนาโนนำไปใช้ในเครื่องสำอาง ดังจะเห็นได้จากการเติบโตอย่างรวดเร็วในการลงทุนและการจดสิทธิบัตรเกี่ยวกับผลิตภัณฑ์ที่เกี่ยวข้องกับอนุภาคนาโนเพื่อการใช้ทางผิวหนัง ตัวอย่างเช่น ในผลิตภัณฑ์กันแดด ผลิตภัณฑ์เพื่อให้ความชุ่มชื้นแก่ผิว แต่อย่างไรก็ตามการเพิ่มขึ้นอย่างรวดเร็วในการใช้ผลิตภัณฑ์ที่มีอนุภาคนาโนเป็นส่วนประกอบนี้ควรได้รับการตรวจสอบเพื่อให้ทราบถึงประสิทธิภาพและความปลอดภัยของผลิตภัณฑ์ก่อนนำไปใช้ด้วย ในบทนี้จะกล่าวถึงการเตรียมอนุภาคนาโนในรูปแบบ ลิโพโซม (Liposomes)(2)
ลิโพโซม (Liposomes)
คืออนุภาคที่มีขนาดเล็กกว่าระดับไมครอน (submicron) มีลักษณะเป็นถุงกลม ๆ ของสารไขมัน โดยสารไขมันเหล่านี้เป็นสารชนิดแอมฟิพาติก (amphipathic) กล่าวคือมีทั้งกลุ่มมีขั้ว (polar) ชอบน้ำและกลุ่มที่ไม่ชอบน้ำในโมเลกุล (hydrophobic) ซึ่งส่วนใหญ่เป็นไขมันประเภท phospholipids ทั้งจากธรรมชาติและสังเคราะห์ขึ้น เช่น phosphatidyl-choline (lecithin), phosphatidyl-ethanolamine, phosphatidyl-glycerol และ phosphatidyl-ionositol เป็นต้น เมื่อผสมลงในสารละลายน้ำ โมเลกุลของสารไขมันประเภท phospholipids สามารถจัดเรียงตัวเป็นชั้นสลับกับชั้นโมเลกุลของน้ำในสารละลายน้ำได้ เพราะโครงสร้างโมเลกุลประกอบด้วยทั้งส่วนมีขั้ว (polar) ชอบน้ำ (hydrophilic) และส่วนที่ไม่มีขั้ว (nonpolar) ไม่ชอบน้ำ (hydrophobic) เมื่ออยู่ในน้ำจะจัดเรียงตัวโดยนำส่วนที่มีขั้วหรือมีประจุหันออกหาโมเลกุลน้ำ ในขณะเดียวกันจะเอาส่วนที่ไม่มีขั้วหันเข้าหาส่วนที่ไม่มีขั้วของโมเลกุลพวกเดียวกัน โดยจะอยู่ในลักษณะของการเรียงตัวเป็นแถวของโมเลกุลไขมันซ้อนกันเป็นผนังสองชั้นหรือ lipid bilayer หากลิโพโซมมี lipid bilayer เพียงชั้นเดียว จะจัดเป็นลิโพโซมประเภท unilamellar bilayer vesicles (ULVs) หากลิโพโซมมี lipid bilayer มากกว่าหนึ่งชั้น (โดยมีชั้นของสารละลายน้ำกั้นอยู่ระหว่างผนังสองชั้น) จะจัดเป็นลิโพโซมประเภท multilamellar bilayer vesicles (MLVs) ตัวยาหรือสารสำคัญที่มีคุณสมบัติชอบน้ำจะกักเก็บอยู่ในส่วนของชั้นที่มีขั้ว ส่วนตัวยาหรือสารสำคัญที่มีคุณสมบัติไม่ชอบน้ำจะแทรกอยู่ใน lipid bilayer โดยทั่วไปตัวยาหรือสารสำคัญที่มีคุณสมบัติชอบน้ำจะถูกกักเก็บในลิโพโซมได้มากกว่าพวกที่มีคุณสมบัติไม่ชอบน้ำ(2) รูปตัวอย่างแสดงดังรูปที่ 1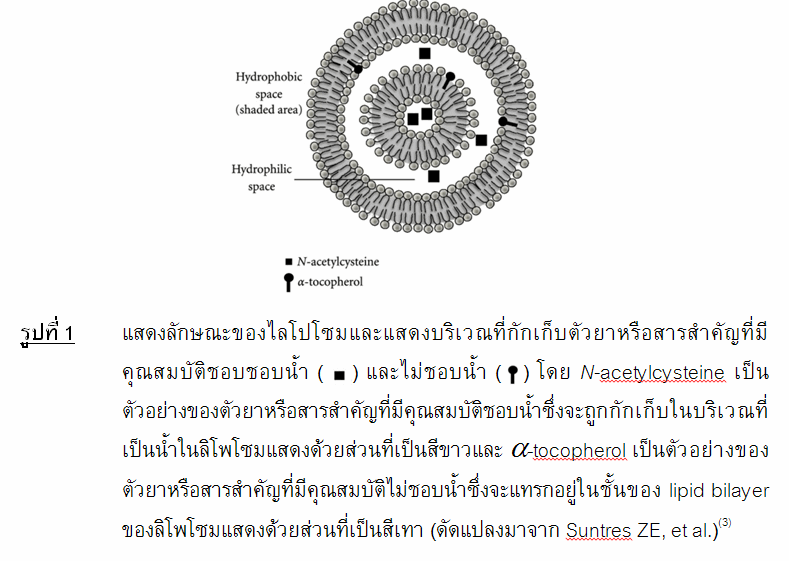
ลิโพโซมส่วนใหญ่จะมีขนาดอยู่ในช่วง 50 นาโนเมตรจนถึงหลายร้อยนาโนเมตร โดยสามารถแบ่งประเภทออกได้ตามขนาดของอนุภาคหรือตามจำนวนชั้นของ lipid bilayer ถ้าแบ่งตามขนาดของอนุภาคจะแบ่งได้เป็น (1) small unilamellar vesicles (SUVs) โดยอนุภาคจะมีขนาดประมาณ 25-50 นาโนเมตร และ (2) large unilamellar vesicles (LUVs) โดยอนุภาคจะมีขนาดใหญ่กว่า 100 นาโนเมตร หรือถ้าแบ่งตามจำนวนชั้นของ lipid bilayer จะแบ่งได้เป็น (1) multilamella vesicles (MLVs) คือลิโพโซมที่มี lipid bilayer มากกว่าหนึ่งชั้น และ (2) unilamellar vesicles (ULVs) คือลิโพโซมที่มี lipid bilayer เพียงหนึ่งชั้น(2) รูปตัวอย่างแสดงดังรูปที่ 2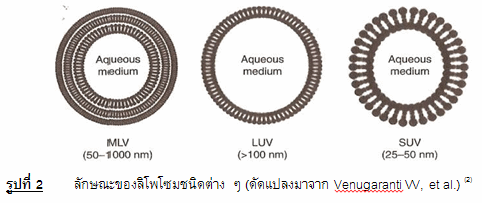
ลิโพโซมมีวิธีการเตรียมได้หลายวิธี เช่น วิธีอัลตร้าซาวน์ (ultrasound), วิธีปั่นผสมเป็นเนื้อเดียวกันด้วยความดันสูง (high-pressure homogenization), วิธีการอัดรีดผ่านแผ่นกรอง (extrusion), วิธีฉีดด้วยตัวทำละลาย (solvent injection method), วิธีทินฟิล์มไฮเดรชั่น (thin-film hydration method) และ วิธีระเหยกลับวัฏภาค (reverse phase evaporation)(4)
กลไกการนำส่งตัวยาหรือสารสำคัญมีหลายกลไก ได้แก่ (1) ลิโพโซมจะถูกดูดซับและหลอมบนผิวหนังและเกิดการซึมผ่านของตัวยาหรือสารสำคัญที่มีคุณลักษณะชอบไขมัน (2) ลิโพโซมจะซึมผ่านผิวหนังทางช่องเปิดหรือท่อบนผิวหนัง (appendageal pathways) หลอมรวมไปกับไขมันในผิวหนัง (sebum) และปล่อยตัวยาหรือสารสำคัญออกมา
ปัจจุบันมีการศึกษาวิจัยในการนำส่งตัวยาหรือสารสำคัญด้วยลิโพโซมมากมาย หลายการศึกษาพบว่าการนำส่งด้วยลิโพโซมสามารถนำส่งตัวยาหรือสารสำคัญสู่ตำแหน่งของผิวหนังบริเวณที่ต้องการได้มากกว่านำส่งในรูปแบบอื่น ๆ เช่น รูปแบบยาน้ำใสทั่วไป, ยาน้ำแขวนตะกอน หรือรูปแบบเจล นอกจากนี้ยังสามารถนำส่งตัวยาหรือสารสำคัญสู่บริเวณผิวที่มีปัญหาเช่น โรคสะเก็ดเงิน (psoriasis), ติดเชื้อรา (mycosis), บริเวณที่มีขนดก (idiophatic hirsutism) และบริเวณผิวที่มีการติดเชื้ออื่น ๆ ได้ เนื่องจากลิโพโซมสามารถกักเก็บตัวยาไว้ในถุงได้ในปริมาณสูงจึงมีประโยชน์ในการนำส่งตัวยาหรือสารสำคัญเฉพาะที่บนผิวหนัง ทำให้สามารถลดขนาดยาลงแลลดการเกิดอาการระคายเคืองบริเวณผิวหนัง ตัวอย่างของตัวยาที่มีการศึกษาการนำส่งด้วยลิโพโซมบริเวณผิวหนัง(2) แสดงดังตารางที่ 1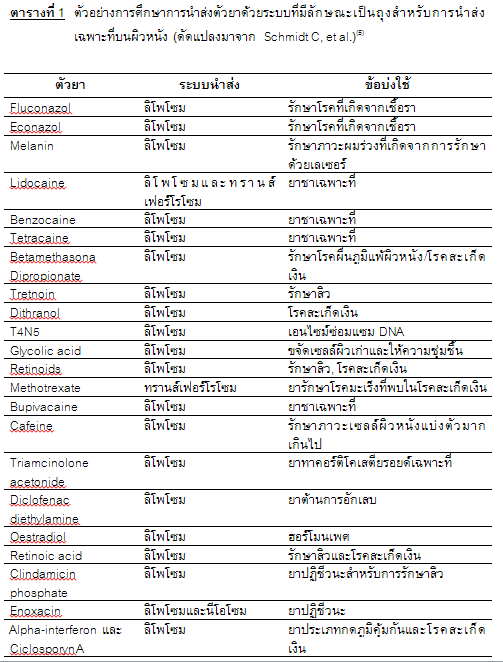
สารต้านอนุมูลอิสระ (antioxidants) ก็มีการศึกษาวิจัยในการนำส่งด้วยลิโพโซมและพบว่าสามารถให้ผลการรักษาที่ดีในภาวะ oxidative stress (ภาวะที่มีอนุมูลอิสระมากมายเสียจนสารต้านอนุมูลอิสระมีไม่เพียงพอและจากสาเหตุดังกล่าวส่งผลให้เกิดการทำลายดีเอ็นเอ โปรตีน ไขมัน และโมเลกุลขนาดเล็กอื่นๆ) เป็นสาเหตุ เนื่องจากสารต้านอนุมูลอิสระเองไม่สามารถผ่านเยื่อหุ้ม พลาสม่า (plasma membrane) ของเซลล์ได้ มีความคงตัวต่ำและค่าครึ่งชีวิตที่สั้นในพลาสม่า การนำส่งด้วยลิโพโซมจึงเป็นการช่วยนำส่งสารต้านอนุมูลอิสระได้อย่างมีประสิทธิภาพที่ดียิ่งขึ้นและสามารถให้ผลทั้งในการป้องกันและรักษาภาวะที่เกิดจาก oxidative stress เป็นสาเหตุได้(3) เช่น การศึกษาการนำส่ง Coenzyme Q10 (CoQ10) ด้วยลิโพโซมใน in vivo พบว่าสามารถเพิ่มการแทรกผ่านของ CoQ10 ผ่านชั้นสตราตัมคอร์เนียมเมื่อเทียบกับตำรับยาน้ำแขวนตะกอน(6)
การประยุกต์ใช้ไลโปโซมทางเวชสำอาง
การประยุกต์ใช้ไลโปโซมเพื่อช่วยเพิ่มความคงตัวของสารสำคัญทางเวชสำอาง
สารสำคัญทางเวชสำอางบางชนิดมีความคงตัวต่ำ เช่น เอนไซม์ โปรตีนและสารต้านปฎิกิริยาออกซิเดชัน (antioxidant) เช่น วิตามินซีและวิตามินอี ไลโปโซมช่วยป้องกันสารสำคัญเหล่านี้จากการสลายตัวในสภาวะแวดล้อม(7) Ioele และคณะ(8) ศึกษาการสลายตัวจากแสง (photodegradation) ของ retinoic acid (tretinoin และ isotretinoin) ที่เตรียมในรูปแบบของสารละลายเอธานอลและไลโปโซม โดยใช้แสงจากหลอดซีนอน (xenon lamp) ในช่วงความยาวคลื่น 300-800 นาโนเมตร จากการศึกษาพบว่า tretinoin ในรูปแบบของสารละลายเอธานอลสลายตัวเป็น 13-cis-retinoic acid และ isotretinoin acid สลายตัวเป็น 9-cis-retinoic acid อย่างรวดเร็ว แล้ว 13-cis-retinoic จึงค่อยๆเปลี่ยนเป็น 9-cis-retinoic acid อย่างช้าๆ แต่ tretinoin และ isotretinoin ในรูปแบบไลโปโซมมีความคงตัวมากกว่า
การประยุกต์ใช้ไลโปโซมเพื่อช่วยเพิ่มการซึมผ่านผิวหนังของสารสำคัญ
จากส่วนประกอบและโครงสร้างของไลโปโซมที่คล้ายคลึงกับผิวหนัง จึงสามารถซึมผ่านผิวหนังได้ดีกว่าระบบนำส่งชนิดอื่น(9) Padamwar และ Pokharkar(10) เตรียมไลโปโซมที่เก็บกัก vitamin E acetate โดยวิธีการฉีดด้วยเอธานอล (ethanol injection method) แล้วนำไปเตรียมต่อในรูปแบบเจล จากการศึกษาการสะสมของ vitamin E acetate ในผิวหนังหนูโดยใช้ Franz Diffusion cell พบว่า สูตรตำรับที่ประกอบด้วยไลโปโซมให้การสะสมของ vitamin E acetate ในผิวหนังมากกว่าสูตรที่ไม่มีไลโปโซมถึง 7 เท่าและเมื่อเปรียบเทียบไลโปโซมของ vitamin E acetate ที่เตรียมในรูปแบบเจลกับเจลเปล่าและ vitamin E acetate ในรูปแบบครีมที่มีขายในท้องตลาด พบว่าไลโปโซมในรูปแบบเจลให้การสะสมของ vitamin E acetate ในผิวหนังที่มากกว่า 6 และ 4 เท่าตามลำดับ
การประยุกต์ใช้ไลโปโซมเพื่อช่วยกักเก็บน้ำในผิวหนัง
ไลโปโซมสามารถช่วยป้องกันการระเหยของน้ำออกจากผิวหนังโดยไขมันที่เป็นส่วนประกอบของไลโปโซมจะแผ่เป็นฟิล์มปกคลุมผิวหนังไว้(11) Betz และคณะ(8) ศึกษาผลของไลโปโซมที่มีต่อการรักษาความชุ่มชื้นของผิวหนัง โดยการเปรียบเทียบไลโปโซมที่เตรียมจากฟอสโฟลิปิดที่ได้จากไข่และถั่วเหลือง ทำการทดสอบที่ท้องแขนของอาสาสมัคร 10 คน อายุระหว่าง 24-32 ปี จากการศึกษาพบว่าไลโปโซมที่เตรียมจากฟอสโฟลิปิดที่ได้จากไข่มีประสิทธิภาพในการรักษาความชื้นบนผิวหนังมนุษย์ที่สูงกว่าเมื่อเปรียบเทียบกับไลโปโซมที่เตรียมจากฟอสโฟลิปิดที่ได้จากถั่วเหลืองและการลดฟอสโฟลิปิดในลิโปโซมลงจะลดประสิทธิภาพในการรักษาความชื้นบนผิวหนังมนุษย์ นอกจากนี้ยังพบว่าไลโปโซมที่เตรียมจากฟอสโฟลิปิดที่ได้จากไข่และถั่วเหลืองที่มีความเข้มข้นของไขมัน 1 และ 2 เปอร์เซ็นต์มีประสิทธิภาพในการเพิ่มความชื้นบนผิวหนังหลังจากการใช้
การประยุกต์ใช้ไลโปโซมเพื่อลดการระคายเคืองจากสารสำคัญทางเวชสำอาง
การกักเก็บสารสำคัญที่ก่อให้เกิดการระคายเคืองไว้ในไลโปโซมจะช่วยลดการสัมผัสของสารกับผิวหนัง(11) และ ควบคุมการปลดปล่อยสารสำคัญให้อยู่ในระดับที่ไม่ก่อให้เกิดการระคายเคือง(9) จึงช่วยลดการระคายเคืองลงได้ Perugini และคณะ(12) ศึกษาความสามารถในการลดการระคายเคืองของ glycolic acid เมื่อพัฒนาให้อยู่ในรูปของไลโปโซมและไมโครสเฟียส์ (microsphere) โดยจากการศึกษาพบว่า ไลโปโซมสามารถควบคุมการปลดปล่อย glycolic acid ให้ช้าลงได้ โดยสัดส่วนระหว่าง glycolic acid และไขมันที่ดีที่สุด คือ 5 ต่อ 1 ในหน่วยอัตราส่วนโมลาร์ (molar ratio) ส่วนไมโครเปียส์ที่เตรียมจากไคโตแซน (chitosan) ไม่สามารถควบคุมการปลดปล่อยของ glycolic acid ได้
บทสรุป
ในปัจจุบันได้มีการพัฒนาเครื่องสำอางให้มีประสิทธิภาพมากขึ้นโดยมีการใส่สารสำคัญลงไปในผลิตภัณฑ์เพื่อให้มีการออกฤทธิ์เชิงรักษาเรียกว่า ‘เวชสำอาง’ อีกทั้งได้มีแนวทางการพัฒนาตำรับเวชสำอางให้มีประสิทธิภาพดียิ่งขึ้นด้วยการใช้ระบบนำส่ง โดยเฉพาะการใช้อนุภาคนาโนในผลิตภัณฑ์ ทั้งนี้ผิวหนังเป็นเครื่องกีดขวางที่สำคัญในการซึมแพร่ผ่านของสารสำคัญ ข้อมูลของสารสำคัญเช่น คุณสมบัติทางเคมีกายภาพ รวมทั้งกลไกการออกฤทธิ์และชั้นผิวหนังของที่เป็นเป้าหมายในการออกฤทธิ์เป็นข้อมูลสำคัญในการเลือกวิธีนำส่งสารสำคัญเข้าสู่ชั้นของผิวหนัง การเลือกใช้วิธีนำส่งสารสำคัญที่เหมาะสมจะเป็นการเพิ่มประสิทธิภาพในการซึมแพร่ผ่านของสารสำคัญ ประหยัดและปลอดภัยแก่ผู้ใช้ ข้อได้เปรียบในการนำส่งสารสำคัญเหล่านี้โดยการกักเก็บไว้ในระบบนำส่งอนุภาคนาโนคือ ความสามารถในการเพิ่มการดูดซึม, เพิ่มการละลาย, สามารถป้องกันการเสื่อมสลาย, ควบคุมการปลดปล่อยสารสำคัญ, หรือทำให้เกิดความรู้สึกสัมผัสที่ดีบนผิวหนังหลังจากใช้ผลิตภัณฑ์ ฯลฯ อนุภาคนาโนที่สามารถนำมาใช้มีอยู่ในหลายรูปแบบขึ้นอยู่กับส่วนประกอบของอนุภาค, วิธีที่ใช้ผลิต, สารสำคัญที่ต้องการกักเก็บ, กลไกการนำส่งอนุภาคที่ต้องการ ซึ่งปัจจัยเหล่านี้อาจกำหนดสมบัติทางเคมีกายภาพของอนุภาคนาโน เช่น ขนาดอนุภาค, พื้นผิวอนุภาค, และความคงตัวของอนุภาคเป็นต้น
ในท้องตลาดได้มีผลิตภัณฑ์ที่มีอนุภาคนาโนเป็นระบบนำส่ง เช่น Cutanova Cream NanoVital Q10, SURMER Cr?me Leg?re Nano-Protection ซึ่งสามารถนำส่งสารสำคัญได้อย่างมีประสิทธิภาพดีกว่าตำรับเครื่องสำอางแบบเก่า เช่น ครีม หรือ อิมัลชั่น นอกจากนี้ยังทำให้ผลิตภัณฑ์มีความน่าสนใจและเป็นการเพิ่มมูลค่าให้กับผลิตภัณฑ์อีกด้วย
อย่างไรก็ตามการพัฒนาระบบนำส่งอนุภาคนาโน นอกเหนือจากการทดสอบถึงลักษณะทางเคมีกายภาพและความคงสภาพของอนุภาคนาโน ผู้พัฒนาต้องคำนึงถึงประสิทธิภาพและความปลอดภัยของผลิตภัณฑ์ก่อนที่จะนำไปใช้ต่อไป