ความบกพร่องของท่อประสาท (neural tube defects) เป็นความผิดปกติแต่กำเนิดที่เกิดกับท่อประสาทที่ไขสันหลังหรือสมอง ความบกพร่องที่พบบ่อยเป็นชนิดท่อประสาทไม่ปิด โดยเฉพาะอย่างยิ่งภาวะกระดูกสันหลังโหว่ (spina bifida) ซึ่งเกิดความพิการไปตลอดชีวิต และภาวะกะโหลกศีรษะไม่ปิด (anencephaly) หรือสภาพที่ไร้สมองใหญ่ซึ่งทารกมักเสียชีวิต สาเหตุสำคัญที่ทำให้เกิดความบกพร่องของท่อประสาทคือการขาดโฟเลต (วิตามินบี 9) ในช่วงที่มารดาตั้งครรภ์ และอาจรวมถึงการขาดวิตามินบี 12 ด้วย ส่วนสาเหตุอื่นพบได้บ้าง เช่น พันธุกรรม การสูบบุหรี่ช่วงตั้งครรภ์ การได้รับยาบางชนิดช่วงตั้งครรภ์ เช่น opioids, valproic acid (ดูข้อมูลเพิ่มเติมได้ในเรื่อง “Valproate…เพิ่มมาตรการจำกัดการใช้ในสตรีวัยเจริญพันธุ์” ใน “ข่าวยา” ประจำสัปดาห์ที่ 4 เดือน เมษายน ปี 2560 ได้ที่
https://pharmacy.mahidol.ac.th/dic/news_week_full.php?id=1397 และเรื่อง “Valproic acid ไม่ปลอดภัยในหญิงมีครรภ์” ใน “ข่าวยา” ประจำสัปดาห์ที่ 3 เดือน ธันวาคม ปี 2557 ได้ที่
https://pharmacy.mahidol.ac.th/dic/news_week_full.php?id=1254) และเมื่อเร็วๆ นี้ มีรายงานถึงความเสี่ยงต่อความบกพร่องของท่อประสาทในทารกที่มารดารับประทาน dolutegravir ในช่วงต้นของการตั้งครรภ์
Dolutegravir เป็นยาในกลุ่ม antiretroviral drugs ใช้รักษาโรคติดเชื้อเอชไอวี (HIV) ในผู้ใหญ่และเด็กที่มีอายุกว่า 12 ปี โดยใช้ร่วมกับยาต้านเอชไอวีชนิดอื่น ยานี้ออกฤทธิ์ขัดขวางการกระจายของไวรัส โดยออกฤทธิ์ยับยั้งเอนไซม์ integrase (ดูข้อมูลเพิ่มเติมได้ในเรื่อง “Integrase inhibitors...จากยาเดี่ยวมาสู่ยาสูตรผสม” ใน “ข่าวยา” ประจำสัปดาห์ที่ 3 เดือน มีนาคม ปี 2558 ได้ที่
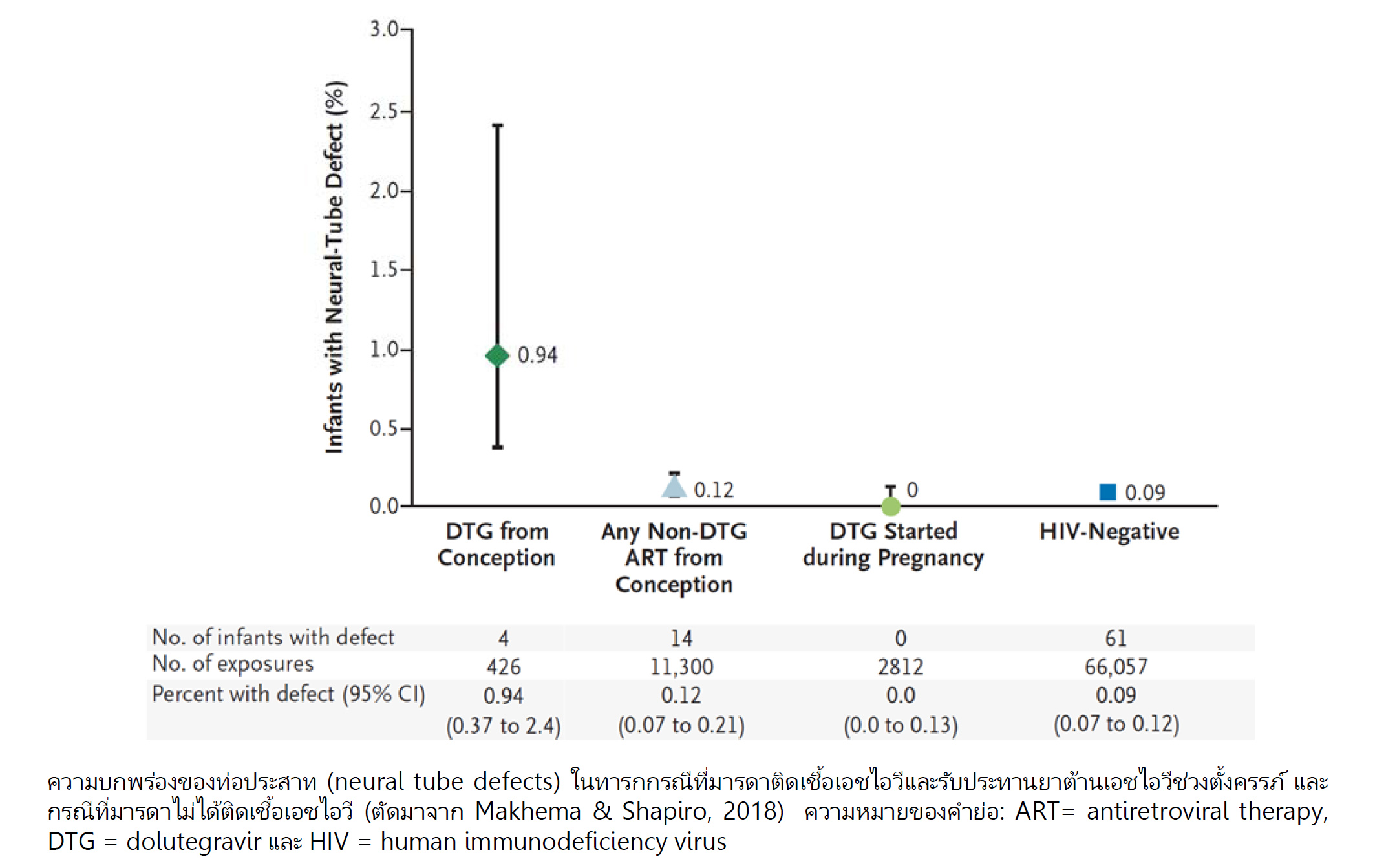
https://pharmacy.mahidol.ac.th/dic/news_week_full.php?id=1272) จากผลการศึกษาที่ Botswana (Tsepamo Study) ในเบื้องต้นพบว่าทารกที่คลอดจากมารดาที่ติดเชื้อเอชไอวีและมารดาเริ่มรับประทาน dolutegravir ตั้งแต่มีการปฏิสนธิ (เริ่มตั้งครรภ์) นั้น มีความบกพร่องของท่อประสาทได้ 0.94% (4 คน จากจำนวนทารก 426 คน) ในขณะที่พบเพียง 0.12% (14 คน จากจำนวนทารก 11,300 คน) ของทารกที่คลอดจากมารดาที่เริ่มรับประทานยาต้านเอชไอวีชนิดอื่นตั้งแต่มีการปฏิสนธิ แต่ไม่พบทารกที่มีความผิดปกติดังกล่าว (0 คน จากจำนวนทารก 2,812 คน) หากมารดาเริ่มรับประทาน dolutegravir ในช่วงถัดมาของการตั้งครรภ์ ในขณะที่ความบกพร่องของท่อประสาทพบได้ 0.09% (61 คน จากจำนวนทารก 66,057 คน) ของทารกที่คลอดจากมารดาที่ไม่ติดเชื้อเอชไอวี (ดูรูป) ขณะนี้ยังรอผลการศึกษาที่สมบูรณ์ซึ่งคาดว่าจะเสร็จในปีหน้า
จากผลการศึกษาเบื้องต้นดังที่กล่าวมา ซึ่งพบว่าความเสี่ยงต่อความบกพร่องของท่อประสาทในทารกมีสูงขึ้นหากมารดาเริ่มรับประทาน dolutegravir ตั้งแต่ช่วงที่มีการปฏิสนธิ (เริ่มตั้งครรภ์) ซึ่งช่วงไตรมาสแรกของการตั้งครรภ์เป็นช่วงที่เริ่มมีการสร้างไขสันหลัง สมอง และโครงสร้างอื่นของระบบประสาท ในขณะที่ไม่พบความบกพร่องของท่อประสาทหากมารดาเริ่มรับประทาน dolutegravir ในช่วงถัดมาของการตั้งครรภ์ ทำให้เมื่อเร็วๆ นี้องค์กรที่เกี่ยวข้องกับการติดตามความปลอดภัยในการใช้ยา เช่น FDA ของสหรัฐอเมริกา หน่วยงาน Pharmacovigilance Risk Assessment Committee (PRAC) ของ European Medicines Agency (EMA) และหน่วยงาน Medicines and Healthcare Products Regulatory Agency (MHRA) ของสหราชอาณาจักร ได้มีคำเตือนที่สอดคล้องกันเกี่ยวกับการใช้ dolutegravir ในช่วงตั้งครรภ์ โดยมีข้อแนะนำสำหรับผู้ป่วยและบุคลากรทางการแพทย์ (แล้วแต่กรณี) สรุปได้ดังนี้
• ควรพิจารณาให้ยาต้านเอชไอวีชนิดอื่นที่ไม่ใช่ dolutegravir ในสตรีที่จะมีการตั้งครรภ์ เนื่องจากยามีความเสี่ยงต่อความบกพร่องของท่อประสาทในทารก
• อธิบายให้สตรีวัยที่พร้อมจะมีบุตรได้ทราบถึงประโยชน์จากการใช้ dolutegravir เทียบกับความเสี่ยงที่มีต่อทารกในครรภ์
• สตรีวัยที่พร้อมจะมีบุตร ควรทดสอบว่าไม่ได้ตั้งครรภ์ก่อนที่จะเริ่มใช้ dolutegravir และแนะนำให้ใช้การคุมกำเนิดที่มีประสิทธิภาพตลอดช่วงที่รับประทานยา
• สตรีที่รับประทาน dolutegravir อยู่แล้วหากเกิดการตั้งครรภ์ขึ้น ในช่วงไตรมาสแรกควรเปลี่ยนไปใช้ยาอื่นเว้นแต่ว่าจะไม่มียาอื่นให้เลือกใช้ และสตรีที่รับประทาน dolutegravir อยู่แล้ว ไม่ควรหยุดยาเองโดยไม่ได้ปรึกษาบุคลากรทางการแพทย์ เพราะอาจทำให้การติดเชื้อรุนแรงขึ้น
• ข้อแนะนำการใช้ยา dolutegravir ในสตรีที่ตั้งครรภ์ อาจมีการปรับปรุงข้อมูลใหม่ตามความจำเป็นภายหลังการศึกษาที่กล่าวถึงข้างต้นสิ้นสุดลงอย่างสมบูรณ์
อ้างอิงจาก:
(1) FDA Drug Safety Communication: FDA to evaluate potential risk of neural tube birth defects with HIV medicine dolutegravir (Juluca, Tivicay, Triumeq) (May 18, 2018).
https://www.fda.gov/Drugs/DrugSafety/ucm608112.htm; (2) European Medicines Agency. New study suggests risk of birth defects in babies born to women on HIV medicine dolutegravir. 18 May 2018, EMA/295960/2018. (3) Dolutegravir (Tivicay, Triumeq, Juluca): signal of increased risk of neural tube defects; do not prescribe to women seeking to become pregnant; exclude pregnancy before initiation and advise use of effective contraception. Drug Safety Update volume 11 issue 10; June 2018: 1; (4) Makhema J, Shapiro RL. Neural-tube defects with dolutegravir treatment from the time of conception. N Engl J Med 2018. doi: 10.1056/NEJMc1807653.

