โควิด-19 (COVID-19) เป็นโรคติดเชื้อที่ทางเดินหายใจ เกิดจากโคโรนาไวรัสสายพันธุ์ใหม่ คือ “2019-nCoV (2019 novel coronavirus)” หรือ “SARS-CoV-2” เริ่มเกิดการระบาดที่เมืองอู่ฮั่นในประเทศจีน (Wuhan, China) เมื่อเดือนธันวาคมปี พ.ศ. 2562 (ค.ศ. 2019) ปัจจุบันยังคงมีการระบาดอย่างกว้างขวางในหลายประเทศทั่วโลกรวมถึงประเทศไทย อีกทั้งยังพบการกลายพันธุ์อย่างรวดเร็วของไวรัสที่ก่อโรค ผู้ป่วยโควิด-19 มีอาการเกิดขึ้นได้หลายอย่าง เช่น มีไข้ ไอ หายใจลำบาก ปวดศีรษะ ปวดข้อ ปวดกล้ามเนื้อ จมูกไม่ได้กลิ่น เจ็บคอ ปอดอักเสบ อ่อนล้า คลื่นไส้ อาเจียน เบื่ออาหาร ท้องเดินรุนแรง หรือบางรายอาจไม่แสดงอาการใด กรณีที่ผู้ป่วยไม่แสดงอาการใดอาจทำให้ตัวผู้ป่วยเองรวมถึงคนรอบข้างขาดความระมัดระวังและอาจเป็นสาเหตุหนึ่งที่ทำให้โรคมีการระบาดรุนแรงขึ้น อาการของโรคเกิดภายใน 2-14 วันหลังจากได้รับเชื้อ SARS-CoV-2 มีผู้เสียชีวิตเป็นจำนวนมากเนื่องจากการหายใจล้มเหลวและอาการแทรกซ้อนอื่น การคิดค้นยาเพื่อกำจัดไวรัสที่เป็นต้นเหตุและการพัฒนาวัคซีนเพื่อป้องกันโรคดำเนินอยู่อย่างต่อเนื่อง กรณีวัคซีนได้เริ่มมีการพัฒนาตั้งแต่ไตรมาสแรกของปี พ.ศ. 2563 การพัฒนาเป็นไปอย่างเร่งด่วนเพื่อให้ได้วัคซีนมาใช้โดยเร็ว ขณะนี้มีวัคซีนโควิด-19 ออกใช้แล้วในประเทศต่าง ๆ ไม่น้อยกว่า 18 ผลิตภัณฑ์ (ข้อมูลวันที่ 3 สิงหาคม พ.ศ. 2564) มีทั้งชนิดที่ได้รับอนุมัติทะเบียนอย่างสมบูรณ์ (full authorization) และชนิดที่ได้รับอนุมัติให้ใช้กรณีฉุกเฉิน (emergency use authorization) ซึ่งการอนุมัติวัคซีนในแต่ละประเทศมีความแตกต่างกัน ในจำนวนวัคซีนเหล่านี้มีเพียงไม่กี่ชนิดที่อยู่ในรายการที่องค์การอนามัยโลกรับรองให้ใช้ในกรณีฉุกเฉิน (WHO's Emergency Use Listing) ซึ่งจะกล่าวถึงในบทความนี้ ข้อมูลที่เกี่ยวกับประสิทธิภาพและความปลอดภัยของวัคซีนโควิด-19 ทั้งหลายรวมถึงวัคซีนที่องค์การอนามัยโลกรับรองเพื่อใช้ในกรณีฉุกเฉินนั้นขณะนี้ข้อมูลยังไม่สมบูรณ์ การศึกษาทางคลินิกยังคงดำเนินอยู่ ด้วยเหตุนี้ข้อมูลด้านประสิทธิภาพและความปลอดภัยของวัคซีนจึงมีการปรับปรุงเป็นระยะ ๆ
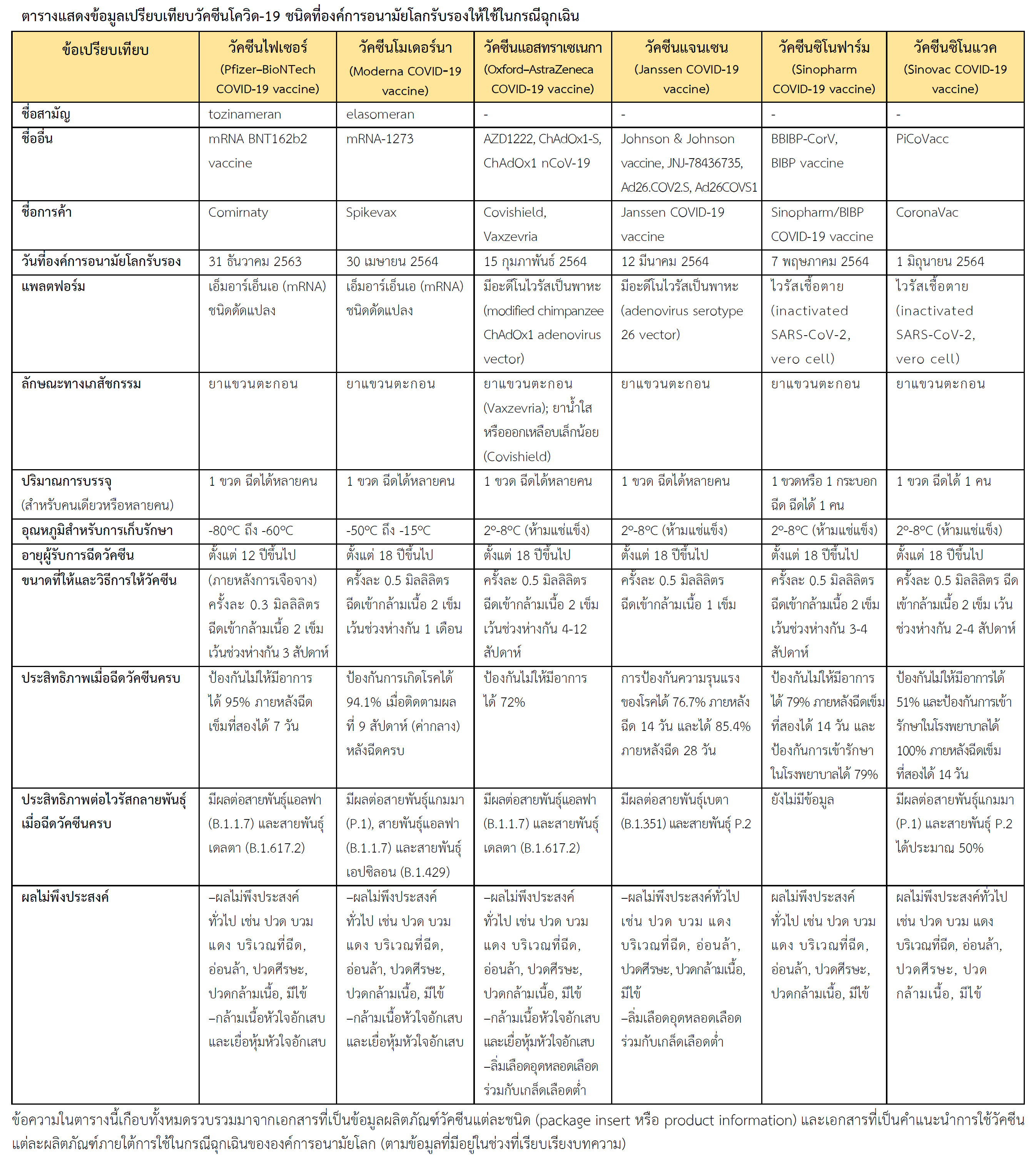
วัคซีนโควิด-19 ที่กล่าวถึงในบทความนี้ วัคซีนโควิด-19 ที่องค์การอนามัยโลกรับรองให้ใช้ในกรณีฉุกเฉินซึ่งจะกล่าวถึงในบทความนี้มี 6 ผลิตภัณฑ์ดังนี้
- วัคซีนไฟเซอร์ (Pfizer–BioNTech COVID-19 vaccine) ชื่อสามัญ: tozinameran, ชื่ออื่น: mRNA BNT162b2 vaccine และชื่อการค้า: Comirnaty
- วัคซีนแอสทราเซเนกา (Oxford–AstraZeneca COVID-19 vaccine) ชื่อรหัส: AZD1222, ชื่ออื่น: ChAdOx1-S, ChAdOx1 nCoV-19 และชื่อการค้า: Covishield และ Vaxzevria
- วัคซีนแจนเซน (Janssen COVID-19 vaccine) หรือวัคซีนจอห์นสันแอนด์จอห์นสัน (Johnson & Johnson COVID-19 vaccine) ชื่อรหัส: JNJ-78436735, ชื่ออื่น: Ad26.COV2.S, Ad26COVS1 และชื่อการค้า: Janssen COVID-19 vaccine
- วัคซีนโมเดอร์นา (Moderna COVID-19 vaccine) ชื่อสามัญ: elasomeran, ชื่อรหัส: mRNA-1273 และชื่อการค้า: Spikevax
- วัคซีนซิโนฟาร์ม (Sinopharm COVID-19 vaccine) ชื่ออื่น: BBIBP-CorV, BIBP vaccine และชื่อการค้า: Sinopharm/BIBP COVID-19 vaccine
- วัคซีนซิโนแวค (Sinovac COVID-19 vaccine) ชื่ออื่น: PiCoVacc และชื่อการค้า: CoronaVac
ผู้ใดควรได้รับการฉีดวัคซีนก่อน ภายใต้สถานการณ์เร่งด่วนอันเนื่องจากการระบาดของโควิด-19 และปริมาณวัคซีนโควิด-19 มีจำกัด องค์การอนามัยโลกมีข้อแนะนำให้บุคคลที่เป็นกลุ่มเสี่ยงต่อการติดเชื้อโควิด-19 หรือมีความเสี่ยงต่อการเกิดโรคที่รุนแรงได้มีโอกาสฉีดวัคซีนก่อนดังนี้ (รวบรวมข้อมูลมาจากเอกสารที่เป็นคำแนะนำการใช้วัคซีนแต่ละผลิตภัณฑ์ภายใต้การใช้ในกรณีฉุกเฉินขององค์การอนามัยโลก ตามข้อมูลที่มีอยู่ในขณะที่เรียบเรียงบทความ ซึ่งรายชื่อโรคที่ระบุในเอกสารสำหรับวัคซีนแต่ละผลิตภัณฑ์มีความแตกต่างกันเล็กน้อย)
- ผู้ที่ควรได้รับการฉีดวัคซีนเป็นอันดับแรก ได้แก่ บุคลากรทางการแพทย์รวมถึงผู้ที่ทำงานใกล้ชิดผู้ป่วยซึ่งมีความเสี่ยงต่อการได้รับเชื้อโควิด-19 และผู้สูงอายุซึ่งเสี่ยงต่อการเกิดโควิด-19 ที่รุนแรงหากเกิดการติดเชื้อ
- ผู้ป่วยด้วยโรคเหล่านี้ซึ่งเสี่ยงต่อการเกิดโควิด-19 ที่รุนแรงหากมีการติดเชื้อเกิดขึ้น ได้แก่ โรคปอดเรื้อรัง โรคหัวใจซึ่งมีอาการ โรคอ้วนรุนแรง โรคเบาหวาน โรคความดันโลหิตสูง โรคตับ โรคติดเชื้อเอชไอวี (human immunodeficiency virus หรือ HIV) ทั้งนี้ควรมีการให้ข้อมูลและให้คำปรึกษากับผู้ป่วยเหล่านี้ ทั้งเรื่องอันตรายของโควิด-19 และผลไม่พึงประสงค์ของวัคซีน
- กลุ่มเสี่ยงอื่น ๆ ที่มีโอกาสติดเชื้อซึ่งต้องเร่งฉีดวัคซีนเช่นกัน หากอยู่ในสถานการณ์ที่ปริมาณวัคซีนมีจำกัด ควรรีบฉีดเข็มแรกให้ครอบคลุมกลุ่มเสี่ยงนี้ให้ได้มากที่สุดก่อน ดังนั้นผู้ที่ได้ฉีดเข็มแรกไปแล้วอาจรอฉีดเข็มที่สองให้นานออกไปแต่ยังอยู่ในช่วงกำหนดระยะห่างของวัคซีนชนิดที่ฉีดเข็มแรกไปแล้ว
- ภายใต้สถานการณ์ที่ปริมาณวัคซีนมีจำกัด หากกลุ่มเสี่ยงเป็นผู้ป่วยโควิด-19 ที่หายแล้วซึ่งคาดว่าภูมิต้านทานยังคงมีอยู่นานถึง 6 เดือน อาจชะลอการฉีดวัคซีนออกไปได้นาน 6 เดือน
แพลตฟอร์มที่ใช้ผลิตวัคซีน แพลตฟอร์ม (platform) ในที่นี้หมายถึงโครงสร้างพื้นฐานของวัคซีนที่เกิดจากกรรมวิธีหรือเทคโนโลยีที่ใช้ผลิตวัคซีน ซึ่งวัคซีนจำนวน 6 ผลิตภัณฑ์ที่กล่าวถึงข้างต้นนั้นมีแพลตฟอร์มที่เป็นเอ็มอาร์เอ็นเอ (messenger ribonucleic acid หรือ mRNA) จำนวน 2 ผลิตภัณฑ์ คือวัคซีนไฟเซอร์และวัคซีนโมเดอร์นา แพลตฟอร์มที่มีอะดีโนไวรัสเป็นพาหะ (adenovirus vector) จำนวน 2 ผลิตภัณฑ์ คือวัคซีนแอสทราเซเนกาและวัคซีนแจนเซน และแพลตฟอร์มที่ใช้เชื้อตาย (inactivated SARS-CoV-2) จำนวน 2 ผลิตภัณฑ์ คือวัคซีนซิโนฟาร์มและวัคซีนซิโนแวค
ลักษณะทางเภสัชกรรม วัคซีนทั้งหมดมีลักษณะเป็นยาแขวนตะกอน (suspension) ยกเว้นวัคซีนแอสทราเซเนกาที่มีชื่อการค้า Covishield มีลักษณะเป็นยาน้ำใสหรือออกเหลือบเล็กน้อย (clear to slightly opaque solution) ผลิตภัณฑ์ที่มีวัคซีนบรรจุในขวดยาสำหรับการใช้ฉีดหลายครั้ง (multiple-dose vial) หรือ 1 ขวดฉีดได้หลายคน ได้แก่ วัคซีนไฟเซอร์ วัคซีนโมเดอร์นา วัคซีนแอสทราเซเนกา และวัคซีนแจนเซน ส่วนวัคซีนซิโนฟาร์มและวัคซีนซิโนแวคบรรจุในขวดยาสำหรับการฉีดให้ 1 คน (single-dose vial) ซึ่งซิโนฟาร์มยังมีชนิดบรรจุในกระบอกฉีดยาแบบพร้อมใช้ (auto-disable prefilled syringe) สำหรับการฉีดให้ 1 คนอีกด้วย คาดว่าในภายหน้าอาจมีผลิตภัณฑ์ที่บรรจุวัคซีนในขวดยาหรือกระบอกฉีดยาสำหรับการฉีดให้ 1 คนออกใช้มากขึ้น
การเก็บรักษา วัคซีนชนิดเอ็มอาร์เอ็นเอทั้งวัคซีนไฟเซอร์และวัคซีนโมเดอร์นาต้องเก็บในสภาพแช่แข็งและเก็บพ้นแสง โดยวัคซีนไฟเซอร์เก็บที่อุณหภูมิ -80
oC ถึง -60
oC ได้นาน 6 เดือน และวัคซีนโมเดอร์นาเก็บที่อุณหภูมิ -50
oC ถึง -15
oC ได้นาน 6 เดือน ส่วนวัคซีนที่เหลือ ได้แก่ วัคซีนแอสทราเซเนกา วัคซีนแจนเซน วัคซีนซิโนฟาร์มและวัคซีนซิโนแวค เก็บที่อุณหภูมิ 2
o-8
oC (ห้ามแช่แข็ง) และเก็บพ้นแสง ซึ่งวัคซีนแอสทราเซเนกาและวัคซีนแจนเซนเก็บได้นาน 6 เดือน ส่วนวัคซีนซิโนฟาร์มเก็บได้นาน 24 เดือน (ที่ขวดมีสติกเกอร์ซึ่งเปลี่ยนสีได้เมื่อถูกความร้อน ช่วยให้รู้ว่าวัคซีนอยู่ในสภาพเดิมหรือไม่) และวัคซีนซิโนแวคเก็บได้นาน 12 เดือน ทั้งนี้ให้ตรวจสอบดูวันหมดอายุที่ระบุไว้บนขวดหรือกระบอกฉีดยาที่บรรจุวัคซีนด้วย
ข้อควรคำนึงเกี่ยวกับวัคซีนที่ต้องเก็บในสภาพแช่แข็ง เนื่องจากอาจประสบปัญหาด้านการเก็บรักษา การควบคุมอุณหภูมิขณะขนส่งและความยุ่งยากในการเตรียมวัคซีนก่อนนำมาฉีด โดยเฉพาะวัคซีนไฟเซอร์ซึ่งต้องมีการเจือจางวัคซีนก่อนฉีด การนำวัคซีนออกจากตู้แช่แข็งจะทำให้อายุวัคซีนสั้นลง และวัคซีนที่หลอมแล้วห้ามนำกลับไปแช่แข็งอีก
การให้วัคซีน วัคซีนทั้งหมดที่กล่าวถึงในที่นี้ให้โดยการฉีดเข้ากล้ามเนื้อ (มักฉีดที่ต้นแขน) ก่อนฉีดวัคซีนหากมีไข้หรือมีอุณหภูมิกายสูงกว่า 38.5
oC ให้เลื่อนการฉีดวัคซีนไปก่อนจนกว่าอาการไข้จะหายไป วัคซีนไฟเซอร์ใช้กับผู้ที่มีอายุตั้งแต่ 12 ปีขึ้นไป (เดิมระบุไว้ที่อายุตั้งแต่ 16 ปีขึ้นไป ต่อมามีการศึกษาเพิ่มเติมในเด็กอายุ 12-15 ปี) ส่วนวัคซีนชนิดอื่นใช้กับผู้ที่มีอายุตั้งแต่ 18 ปีขึ้นไป วัคซีนทุกผลิตภัณฑ์ฉีด 2 เข็ม ยกเว้นวัคซีนแจนเซนฉีดเพียง 1 เข็ม (ตามข้อมูลในขณะนี้) วัคซีนไฟเซอร์เป็นชนิดเดียวที่ต้องเจือจางก่อนฉีดและเป็นวัคซีนชนิดเดียวที่ฉีดเพียง 0.3 มิลลิลิตร ส่วนวัคซีนอื่นฉีด 0.5 มิลลิลิตร
(ดูรายละเอียดในตารางท้ายบทความ) การเว้นระยะห่างระหว่างเข็มแรกและเข็มที่สอง (ซึ่งเป็นเข็มกระตุ้นในกรณีที่ฉีด 2 เข็ม) กำหนดไว้แตกต่างกันดังนี้ วัคซีนไฟเซอร์เว้นห่างกัน 3 สัปดาห์ วัคซีนโมเดอร์นาเว้นห่างกัน 1 เดือน วัคซีนแอสทราเซเนกาเว้นห่างกัน 4-12 สัปดาห์ วัคซีนซิโนฟาร์มเว้นห่างกัน 3-4 สัปดาห์ และวัคซีนซิโนแวคเว้นห่างกัน 2-4 สัปดาห์ เกี่ยวกับการเว้นระยะห่างระหว่างเข็มแรกและเข็มที่สองนั้น ดังได้กล่าวแล้วข้างต้นว่าภายใต้สถานการณ์ที่ปริมาณวัคซีนมีจำกัดและต้องรีบฉีดเข็มแรกให้ครอบคลุมกลุ่มเสี่ยงให้ได้มากที่สุดก่อน ดังนั้นผู้ที่ได้ฉีดเข็มแรกไปแล้วอาจรอฉีดเข็มที่สองให้นานออกไปแต่ยังอยู่ในช่วงกำหนดระยะห่างของวัคซีนชนิดที่ฉีดเข็มแรกไปแล้ว ซึ่งการเว้นระยะห่างระหว่างการฉีดเข็มแรกและเข็มที่สองให้นานขึ้น เช่นกรณีของวัคซีนแอสทราเซเนกาหากเว้นห่างกัน 8-12 สัปดาห์อาจช่วยเพิ่มประสิทธิภาพของวัคซีนได้ กรณีวัคซีนโมเดอร์นาหากมีความจำเป็นอาจเลื่อนฉีดเข็มที่สองไปจนถึง 42 วัน หรือหากประเทศใดประสบปัญหาเรื่องวัคซีนไม่เพียงพออาจเลื่อนไปได้นานถึง 12 สัปดาห์ อย่างไรก็ตามสำหรับวัคซีนชนิดที่ต้องฉีด 2 เข็มประสิทธิภาพจะเกิดเต็มที่ต่อเมื่อได้ฉีดครบทั้ง 2 เข็ม
ประสิทธิภาพในการกระตุ้นภูมิคุ้มกัน ไม่มีการศึกษาที่เปรียบเทียบโดยตรงถึงประสิทธิภาพในการกระตุ้นภูมิคุ้มกันของวัคซีนโควิด-19 แต่ละชนิด การศึกษาถึงประสิทธิภาพของวัคซีนแต่ละชนิดทำในสถานการณ์ต่างกัน ไม่ว่าจะเป็นสถานที่ ความรุนแรงในการระบาดของโรค ช่วงเวลาที่ประเมินประสิทธิภาพหลังจากฉีดวัคซีน อีกทั้งการประเมินประสิทธิภาพอาจประเมินด้านการป้องกันไม่ให้มีอาการ หรือการป้องกันความรุนแรงของโรคซึ่งครอบคลุมถึงการเข้ารักษาตัวในโรงพยาบาล เป็นต้น จากเอกสารที่เป็นคำแนะนำการใช้วัคซีนแต่ละผลิตภัณฑ์ภายใต้การใช้ในกรณีฉุกเฉินขององค์การอนามัยโลก (ตามข้อมูลที่มีอยู่ขณะนี้) ให้ข้อมูลถึงประสิทธิภาพของวัคซีนไฟเซอร์ว่าสามารถป้องกันไม่ให้มีอาการของโควิด-19 ได้ 95% ภายหลังฉีดเข็มที่สองได้ 7 วัน (เข็มแรกและเข็มที่สองฉีดห่างกัน 21 วัน), วัคซีนโมเดอร์นามีประสิทธิภาพในการป้องกันการเกิดโรคได้ 94.1% เมื่อติดตามผลที่ 9 สัปดาห์ (เป็นค่ากลาง) ภายหลังฉีดครบ 2 เข็ม, วัคซีนแอสทราเซเนกามีประสิทธิภาพในการป้องกันไม่ให้มีอาการของโควิด-19 ได้ 72% ภายหลังการฉีดครบ 2 เข็มซึ่งห่างกัน 4-12 สัปดาห์ และพบว่าการเว้นช่วงห่างระหว่างเข็มแรกและเข็มที่สองให้นานขึ้นมีแนวโน้มว่ามีประสิทธิภาพดีขึ้น, วัคซีนแจนเซนมีประสิทธิภาพในการป้องกันความรุนแรงของโรคได้ 76.7% ภายหลังฉีด 14 วัน (วัคซีนชนิดนี้ฉีดเพียงเข็มเดียว) และ 85.4% ภายหลังฉีด 28 วัน และทำให้ผู้ป่วยไม่ต้องเข้ารักษาตัวในโรงพยาบาลได้ 93.1% ภายหลังฉีด 14 วัน และได้ 100% ภายหลังฉีด 28 วัน, การฉีดวัคซีนซิโนฟาร์มครบ 2 เข็มซึ่งฉีดห่างกัน 21 วันมีประสิทธิภาพในการป้องกันไม่ให้มีอาการของโควิด-19 ได้ 79% ตั้งแต่ฉีดเข็มที่สองได้ 14 วัน และป้องกันการเข้ารักษาตัวในโรงพยาบาลได้ 79%, ในการศึกษาทางคลินิกระยะที่ 3 ของวัคซีนซิโนแวคในประเทศบราซิลพบว่าการฉีดวัคซีนครบ 2 เข็มซึ่งฉีดห่างกัน 14 วันมีประสิทธิภาพในการป้องกันไม่ให้มีอาการของโควิด-19 ได้ 51% การป้องกันความรุนแรงของโรคได้ 100% และการป้องกันการเข้ารักษาตัวในโรงพยาบาลได้ 100% ซึ่งเห็นผลตั้งแต่ฉีดเข็มที่สองได้ 14 วัน
ประสิทธิภาพต่อไวรัสกลายพันธุ์ ยังไม่มีการศึกษาที่ชัดเจนถึงประสิทธิภาพของวัคซีนในการป้องกันไวรัสโควิด-19 ที่กลายพันธุ์ ประสิทธิภาพประเมินผลจากการฉีดวัคซีนในแหล่งที่มีการระบาดของเชื้อกลายพันธุ์ และผลการทดสอบวัคซีนในห้องปฏิบัติการ ซึ่งในเบื้องต้นคาดว่าวัคซีนไฟเซอร์มีประสิทธิภาพต่อเชื้อกลายพันธุ์ชนิดสายพันธุ์แอลฟา (Alpha: B.1.1.7) และสายพันธุ์เดลตา (Delta: B.1.617.2) โดยเฉพาะเมื่อได้ฉีดครบ 2 เข็ม กรณีวัคซีนโมเดอร์นาพบว่าประสิทธิภาพต่อเชื้อสายพันธุ์เบตา (Beta: B.1.351) ลดลง แต่ประสิทธิภาพต่อเชื้อสายพันธุ์อื่นได้รับผลกระทบน้อย ได้แก่ สายพันธุ์แกมมา (Gamma: P.1), สายพันธุ์แอลฟา และสายพันธุ์เอปซิลอน (Epsilon: B.1.429) ส่วนประสิทธิภาพต่อสายพันธุ์เดลตานั้นยังไม่อาจประเมินได้ ส่วนวัคซีนแอสทราเซเนกามีประสิทธิภาพค่อนข้างดีต่อเชื้อสายพันธุ์แอลฟาและสายพันธุ์เดลตา สำหรับวัคซีนแจนเซนผลการศึกษาทางคลินิกพบว่ามีประสิทธิภาพต่อสายพันธุ์เบตาและสายพันธุ์ P.2 (ก่อนหน้านี้เรียกว่าสายพันธุ์ Zeta ต่อมาไม่ได้รับความสนใจเนื่องจากไม่ใช่สายพันธุ์ที่ก่อการระบาดของโควิด-19) ขณะนี้ยังไม่มีข้อมูลเกี่ยวกับประสิทธิภาพของวัคซีนซิโนฟาร์มต่อเชื้อกลายพันธุ์ กรณีวัคซีนซิโนแวคมีผลจากการศึกษา (observational study) ที่ประมาณการณ์ได้ว่าวัคซีนนี้มีประสิทธิภาพในการป้องกันไม่ให้มีอาการของโควิด-19 จากเชื้อสายพันธุ์แกมมา (ซึ่งพบการระบาดราว 75% ของกลุ่มตัวอย่าง) ได้ 49.6% และจากเชื้อสายพันธุ์ P.2 ได้ 49.6% ภายหลังฉีดเข็มแรกและได้ 50.7% ภายหลังฉีดเข็มที่สองไปแล้ว 2 สัปดาห์ ขณะนี้ยังคงต้องมีการติดตามข้อมูลด้านประสิทธิภาพของวัคซีนชนิดต่าง ๆ ต่อเชื้อกลายพันธุ์อย่างต่อเนื่อง
ผลไม่พึงประสงค์ของวัคซีน ภายหลังการฉีดวัคซีนให้รอดูอาการไม่พึงประสงค์เป็นเวลาไม่น้อยกว่า 15 นาที หากเกิดอาการที่รุนแรงจะได้เข้ารับการรักษาทันทีโดยเฉพาะอย่างยิ่งกรณีที่เกิดการแพ้วัคซีน สำหรับอาการไม่พึงประสงค์โดยทั่วไปเกิดไม่รุนแรง เช่น ปวด บวม แดง คันและมีรอยช้ำบริเวณที่ฉีด ร่างกายอ่อนล้า ปวดศีรษะ ปวดข้อ ปวดกล้ามเนื้อ มีไข้ หนาวสั่น เป็นลม คลื่นไส้ อาเจียน รู้สึกไม่สบาย ต่อมน้ำเหลืองโต ซึ่งอาการส่วนใหญ่เกิดจากปฏิกิริยาการตอบสนองของร่างกายที่มีต่อวัคซีน และเกิดได้ไม่ว่าจะฉีดวัคซีนชนิดใด อาการไม่พึงประสงค์เหล่านี้อาการค่อย ๆ ทุเลาได้เอง สำหรับอาการปวดศีรษะ เป็นไข้ และปวดกล้ามเนื้อสามารถรับประทานยาพาราเซตามอลเพื่อช่วยบรรเทาอาการได้ ส่วนกรณีที่แพ้วัคซีนไม่ว่าจะแพ้ส่วนประกอบใด ๆ ในวัคซีน ซึ่งอาการเกิดขึ้นเร็วหลังฉีดและเกิดอย่างรุนแรง โดยมีผื่นขึ้น ลมพิษ ริมฝีปากและขอบตาบวม หายใจไม่ออก ความดันโลหิตต่ำ ต้องได้รับการรักษาโดยเร็ว ผู้ที่แพ้วัคซีนชนิดใดจะห้ามฉีดวัคซีนชนิดนั้นอีก นอกจากนี้หากเกิดความผิดปกติใด ๆ ในเวลาต่อมา เช่น เจ็บหน้าอก หายใจไม่สะดวก มือและเท้าไม่มีแรง อาเจียนรุนแรง หรืออาการผิดปกติอื่นที่เป็นรุนแรง ให้รีบไปโรงพยาบาลเพื่อรับการวินิจฉัยและการรักษา ผลไม่พึงประสงค์ของวัคซีนไม่ได้จำกัดแค่ที่กล่าวถึงข้างต้น อาจพบผลไม่พึงประสงค์อย่างอื่นได้
สำหรับผลไม่พึงประสงค์บางอย่างซึ่งอาจสัมพันธ์กับแพลตฟอร์มของวัคซีนที่ใช้ (ขณะนี้หลักฐานยังไม่ชัดเจน) เช่น
กล้ามเนื้อหัวใจอักเสบ (myocarditis) และเยื่อหุ้มหัวใจอักเสบ (pericarditis) โดยเฉพาะภายหลังได้รับวัคซีนเข็มที่สอง ความผิดปกตินี้เป็นปฏิกิริยาทางภูมิคุ้มกันเช่นกัน ทำให้เกิดการอักเสบของเนื้อเยื่อดังกล่าวและมีอาการเจ็บหน้าอก หายใจถี่ หรือหัวใจเต้นผิดจังหวะ ส่วนใหญ่มีอาการไม่รุนแรงและทุเลาได้เอง แต่บางรายอาจมีอาการรุนแรงและต้องเข้ารักษาในโรงพยาบาล ความผิดปกติดังกล่าวพบได้ทั้งในผู้ที่ฉีดวัคซีนชนิดเอ็มอาร์เอ็นเอ (วัคซีนไฟเซอร์และวัคซีนโมเดอร์นา) และวัคซีนชนิดที่มีอะดีโนไวรัสเป็นพาหะ (วัคซีนแอสทราเซเนกาและวัคซีนแจนเซน) แต่จากข้อมูลในขณะนี้พบในผู้ที่ฉีดวัคซีนชนิดเอ็มอาร์เอ็นเอได้มากกว่าชนิดที่มีอะดีโนไวรัสเป็นพาหะ ส่วน
ภาวะลิ่มเลือดอุดหลอดเลือดร่วมกับมีเกล็ดเลือดต่ำ (thrombosis with thrombocytopenia syndrome หรือ TTS) นั้น ข้อมูลในขณะนี้พบในผู้ที่ฉีดวัคซีนชนิดที่มีอะดีโนไวรัสเป็นพาหะได้มากกว่าผู้ที่ฉีดวัคซีนชนิดเอ็มอาร์เอ็นเอ ผู้ที่เกิดภาวะลิ่มเลือดอุดหลอดเลือดร่วมกับมีเกล็ดเลือดต่ำอาจมีอาการได้หลากหลาย ขึ้นกับว่ามีลิ่มเลือดไปอุดตันในหลอดเลือดที่อวัยวะใด เช่น ที่ปอด ทำให้เกิดอาการเจ็บหน้าอก หายใจไม่สะดวก เหนื่อย, ที่หัวใจ ทำให้กล้ามเนื้อหัวใจขาดเลือด มีอาการปวดเค้นอก หัวใจเต้นผิดจังหวะ, ที่สมอง ทำให้มีอาการปวดศีรษะรุนแรง ชัก สับสน ตาพร่า ร่างกายชาครึ่งซีก แขนและขาอ่อนแรง, ที่ขา ทำให้ขาบวม แดง และปวดขาข้างที่เกิดหลอดเลือดอุดตัน เป็นต้น หากเกิดความผิดปกติดังกล่าวรวมถึงความผิดปกติอื่น ๆ ที่เป็นรุนแรง ให้รีบไปโรงพยาบาลเพื่อรับการวินิจฉัยและการรักษาโดยเร็ว
การฉีดวัคซีนให้กับผู้หญิงตั้งครรภ์และผู้หญิงที่ให้นมบุตร ผู้หญิงตั้งครรภ์มีความเสี่ยงต่อการเกิดโควิด-19 ที่รุนแรงได้มากกว่าผู้หญิงที่ไม่ได้ตั้งครรภ์ โดยเฉพาะช่วงไตรมาสที่ 2 และไตรมาสที่ 3 หรือผู้หญิงที่ตั้งครรภ์นั้นมีอายุมาก (อายุ 35 ปีหรือมากกว่านี้) หรือมีน้ำหนักตัวมาก หรือมีโรคอื่นร่วม เช่น โรคเบาหวาน โรคความดันโลหิตสูง ข้อมูลด้านประสิทธิภาพและความปลอดภัยของวัคซีนโควิด-19 ในผู้หญิงตั้งครรภ์และผู้หญิงที่ให้นมบุตรยังมีจำกัด ในด้านประสิทธิภาพคาดว่าวัคซีนทุกผลิตภัณฑ์สามารถกระตุ้นภูมิคุ้มกันได้เช่นเดียวกับผู้หญิงที่ไม่ได้ตั้งครรภ์และผู้หญิงที่ไม่ได้ให้นมบุตร ส่วนด้านความปลอดภัยนั้นยังไม่มีข้อมูลว่าผู้หญิงตั้งครรภ์และผู้หญิงที่ให้นมบุตรจะได้รับผลกระทบจากวัคซีนมากกว่าผู้หญิงทั่วไปหรือไม่ ส่วนผลต่อทารกนั้นวัคซีนทั้งหมดที่กล่าวถึงไม่ใช่วัคซีนชนิดเชื้อเป็น (กรณีที่มีอะดีโนไวรัสเป็นพาหะนั้นอนุภาคไวรัสที่นำมาใช้ไม่สามารถแบ่งตัวเพิ่มจำนวนได้) แต่เนื่องจากยังไม่มีข้อมูลด้านความปลอดภัยที่เพียงพอ ด้วยเหตุนี้การฉีดวัคซีนไม่ว่าชนิดใดให้กับผู้หญิงมีครรภ์ควรได้ผ่านการพิจารณาถึงประโยชน์ที่ได้รับจากการฉีดวัคซีนว่ามีมากกว่าความเสี่ยงต่อผลเสียที่อาจเกิดขึ้นกับลูกในท้อง ส่วนผู้หญิงที่ให้นมบุตรยังไม่มีข้อมูลถึงผลกระทบของวัคซีนต่อลูกที่ดื่มนมแม่ อย่างไรก็ตามดังได้กล่าวข้างต้นแล้วว่าวัคซีนทั้งหมดที่กล่าวถึงไม่ใช่วัคซีนชนิดเชื้อเป็น ด้วยเหตุนี้ผู้หญิงที่ให้นมบุตรสามารถฉีดวัคซีนได้และสามารถให้นมบุตรต่อไปได้
วัคซีนป้องกันการแพร่เชื้อได้หรือไม่? ขณะนี้ยังไม่มีข้อมูลว่าวัคซีนทั้ง 6 ชนิดที่กล่าวถึงจะป้องกันการแพร่เชื้อโควิด-19 ได้หรือไม่ ด้วยเหตุนี้แม้ฉีดวัคซีนแล้วยังคงมีข้อแนะนำให้ใส่หน้ากากอนามัย รักษาระยะห่าง หมั่นล้างมือบ่อย ๆ ปิดปากและจมูกเมื่อไอหรือจามด้วยทิชชู ทิ้งทิชชูที่ใช้แล้วลงถังขยะที่ปิดมิดชิด ไม่อยู่ในสถานที่ที่มีคนจำนวนมาก และให้อยู่ในสถานที่ซึ่งมีอากาศถ่ายเทดี
 เอกสารอ้างอิง
เอกสารอ้างอิง - Vaccines in use, last updated 3 August 2021. https://www.covid-19vaccinetracker.org/authorized-vaccines. Accessed: August 4, 2021.
- Fact sheet for healthcare providers administering vaccine (vaccination providers). Emergency use authorization (EUA) of the Pfizer-Biontech COVID-19 vaccine to prevent coronavirus disease 2019 (COVID-19), revised 25 June 2021. https://www.fda.gov/media/144413/download. Accessed: August 2, 2021.
- World Health Organization. Interim recommendations for use of the Pfizer–BioNTech COVID-19 vaccine, BNT162b2, under Emergency Use Listing, updated 15 June 2021. WHO reference number: WHO/2019-nCoV/vaccines/SAGE_recommendation//BNT162b2/2021.2. Accessed: August 2, 2021.
- Pfizer-BioNTech COVID-19 vaccine U.S. distribution fact sheet. https://www.pfizer.com/news/hot-topics/covid_19_vaccine_u_s_distribution_fact_sheet. Accessed: August 2, 2021.
- Fact sheet for healthcare providers administering vaccine (vaccination providers). Emergency use authorization (EUA) of the the Moderna COVID-19 vaccine to prevent coronavirus disease 2019 (COVID-19), revised 24 June 2021. https://www.fda.gov/media/144637/download. Accessed: August 2, 2021.
- World Health Organization. Interim recommendations for use of the Moderna mRNA-1273 vaccine against COVID-19, updated 25 June 2021. WHO reference number: WHO/2019-nCoV/vaccines/SAGE_recommendation/mRNA-1273/2021.2. Accessed: August 2, 2021.
- Moderna announces longer shelf life for its COVID-19 vaccine candidate at refrigerated temperatures. https://investors.modernatx.com/news-releases/news-release-details/moderna-announces-longer-shelf-life-its-covid-19-vaccine/. Accessed: August 2, 2021.
- Vaxzevria suspension for injection, revised 15 July 2021. .https://www.gov.uk/government/publications/regulatory-approval-of-covid-19-vaccine-astrazeneca/information-for-healthcare-professionals-on-covid-19-vaccine-astrazeneca Accessed: August 2, 2021.
- World Health Organization. Interim recommendations for use of the ChAdOx1-S [recombinant] vaccine against COVID-19 (AstraZeneca COVID-19 vaccine AZD1222 VaxzevriaTM, SII COVISHIELDTM), updated 30 July 2021. WHO reference number: WHO/2019-nCoV/vaccines/SAGE_recommendation/AZD1222/2021.3. Accessed: August 2, 2021.
- Global Advisory Committee on Vaccine Safety (GACVS) review of latest evidence of rare adverse blood coagulation events with AstraZeneca COVID-19 Vaccine (Vaxzevria and Covishield), 21 April 2021. https://www.who.int/news. Accessed: August 2, 2021.
- Fact sheet for healthcare providers administering vaccine (vaccination providers) emergency use authorization (EUA) of the Janssen COVID-19 vaccine to prevent coronavirus disease 2019 (COVID-19), revised 8 July 2021. https://www.fda.gov/media/146304/download. Accessed: August 2, 2021.
- World Health Organization. Interim recommendations for the use of the Janssen Ad26.COV2.S (COVID-19) vaccine, updated 15 June 2021. WHO reference number: WHO/2019-nCoV/vaccines/SAGE_recommendation/Ad26.COV2.S/2021.2. Accessed: August 2, 2021.
- COVID-19 Vaccine (Vero Cell), Inactivated (Sinopharm), version 24 May 2021. https://www.who.int/publications/m/item/sinopharm-vero-cell---inactivated-covid-19-vaccine. Accessed: August 2, 2021.
- The Sinopharm COVID-19 vaccine: What you need to know, 10 May 2021. https://www.who.int/news-room/feature-stories/detail/the-sinopharm-covid-19-vaccine-what-you-need-to-know. Accessed: August 2, 2021.
- Recommendation for an emergency use listing of COVID-19 vaccine (vero cell), inactivated submitted by Sinovac, version 28 June 2021. .https://extranet.who.int/pqweb/sites/default/files/documents/SINOVAC_TAG_PEG_REPORT_EUL-Final28june2021.pdf Accessed: August 2, 2021.
- The Sinovac COVID-19 vaccine: What you need to know, 2 June 2021. https://www.who.int/news-room/feature-stories/detail/the-sinovac-covid-19-vaccine-what-you-need-to-know. Accessed: August 2, 2021.
- Doshi P. Covid-19 vaccines: in the rush for regulatory approval, do we need more data? BMJ 2021. doi: 10.1136/bmj.n1244. Accessed: August 2, 2021.
- Research and analysis coronavirus vaccine - weekly summary of Yellow Card reporting updated 30 July 2021. https://www.gov.uk/government/publications/coronavirus-covid-19-vaccine-adverse-reactions/coronavirus-vaccine-summary-of-yellow-card-reporting. Accessed: August 2, 2021.
- Myocarditis and/or pericarditis following COVID-19 vaccines, updated 22 July 2021. https://www.alberta.ca/assets/documents/health-myocarditis-and-pericarditis-following-covid.pdf. Accessed: August 2, 2021.
- Sangli S, Virani A, Cheronis N, Vannatter B, Minich C, Noronha S, et al. Thrombosis with thrombocytopenia after the messenger RNA-1273 vaccine. Ann Intern Med 2021. doi: 10.7326/L21-0244. Accessed: August 2, 2021.