โรคตับอักเสบดี (hepatitis D) เป็นการอักเสบของตับที่เกิดจากการติดเชื้อไวรัส hepatitis D virus (HDV) ที่ต้องอาศัย hepatitis B virus (HBV) ในการจำลองตัวเองเพื่อเพิ่มจำนวนไวรัส โดย HDV จะใช้โปรตีนพื้นผิวของ HBV คือ hepatitis B surface antigen (HBsAg) เป็นโครงสร้างสำคัญในการประกอบไวรัสและบุกรุกเซลล์ตับ ผู้ป่วยที่มีการติดเชื้อ HDV ร่วมกับ HBV จึงมักเกิดโรคตับอักเสบเรื้อรังที่รุนแรงมากจนสามารถพัฒนาไปสู่มะเร็งตับและการเสียชีวิตจากโรคตับได้ ในปัจจุบันยังแนะนำการใช้ pegylated-interferon α (PEG-IFNα) ในการรักษาโรคตับอักเสบดี อย่างไรก็ตามพบว่าการรักษาด้วย PEG-IFNα มีประสิทธิภาพต่ำ เนื่องจากมีเพียง 20-30% ของผู้ป่วยที่ตรวจไม่พบ HDV RNA หลังการรักษา นอกจากนี้ยังมีผลข้างเคียงและข้อห้ามใช้หลายประการซึ่งถือว่าเป็นข้อจำกัดในการรักษา
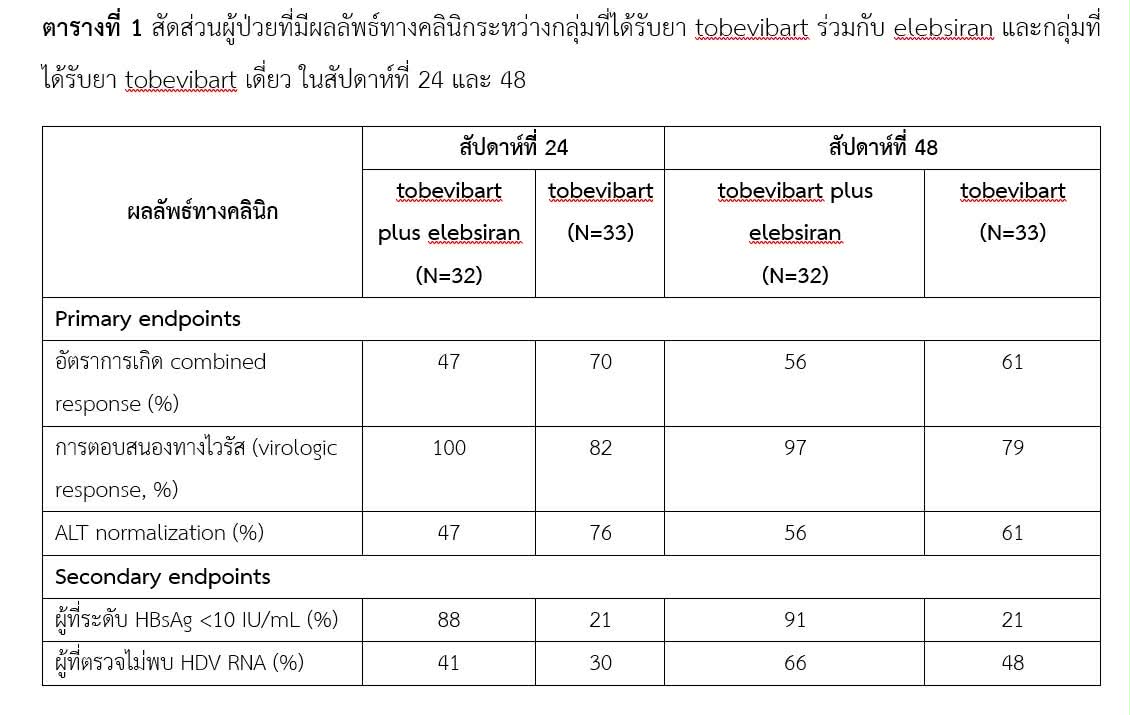
เมื่อวันที่ 9 พฤศจิกายน 2568 วารสาร The New England Journal of Medicine (NEJM) ได้เผยแพร่การศึกษาชื่อ SOLSTICE ซึ่งเป็นการศึกษาทางคลินิก phase II แบบสุ่มที่ใช้ tobevibart ร่วมกับ elebsiran ในการรักษาโรคตับอักเสบดี โดย tobevibart เป็น monoclonal antibody แบบ broad-neutralizing ที่จำเพาะต่อ HBsAg ทำให้สามารถยับยั้งการแพร่กระจายของ HBV และ HDV พร้อมทั้งป้องกันไม่ให้ไวรัสเข้าสู่เซลล์ตับได้อย่างมีประสิทธิภาพ ส่วน elebsiran เป็น small interfering RNA (siRNA) ที่ออกฤทธิ์ยับยั้ง messenger RNA ของ HBV ส่งผลให้การสร้าง HBsAg ลดลง การศึกษานี้มีผู้ป่วยทั้งหมด 65 ราย ได้รับการรักษาด้วย tobevibart ขนาด 300 มิลลิกรัม ร่วมกับ elebsiran ขนาด 200 มิลลิกรัม ทุก 4 สัปดาห์ หรือ tobevibart ขนาด 300 มิลลิกรัม แบบเดี่ยวทุก 2 สัปดาห์ โดยตัวชี้วัดหลักของการศึกษา (primary endpoint) เป็นอัตราการเกิด combined response ที่ประกอบด้วยการตอบสนองทางไวรัส (virologic response) ร่วมกับการมีค่าเอนไซม์ตับปกติ (ALT normalization) ผลการศึกษาในสัปดาห์ที่ 24 พบว่ากลุ่มที่ได้รับ tobevibart ร่วมกับ elebsiran แม้จะมี virological response สูงกว่า แต่ ALT normalization กลับด้อยกว่า ทำให้เมื่อคำนวนพบว่าอัตราการเกิด combined response ต่ำกว่ากลุ่มที่ได้รับ tobevibart แบบเดี่ยว อย่างไรก็ตามในสัปดาห์ที่ 48 อัตราการเกิด combined response ของทั้งสองกลุ่มมีค่าใกล้เคียงกัน รวมทั้งเมื่อพิจารณาผลลัพธ์รอง (secondary endpoint) พบว่ากลุ่มที่ได้รับยาร่วมมีผลลัพธ์ดีกว่ายาเดี่ยวอย่างชัดเจนดังแสดงในตารางที่ 1 ด้านความปลอดภัย เหตุการณ์ไม่พึงประสงค์ที่เกิดขึ้นระหว่างการรักษา (treatment-emergent adverse events; TEAEs) ส่วนใหญ่มีความรุนแรงเล็กน้อยถึงปานกลางและเกิดขึ้นชั่วคราวในทุกกลุ่มการรักษา โดยอาการที่พบได้บ่อยที่สุด คือ อาการคล้ายไข้หวัดและอาการหนาวสั่น โดยการใช้ยาคู่นี้กำลังอยู่ในขั้นตอนการศึกษาเพิ่มเติมใน phase III ชื่อ ECLIPSE เพื่อประเมินความปลอดภัย ประสิทธิภาพ และผลลัพธ์ทางคลินิกในระยะยาวในผู้ป่วยที่ติดเชื้อ HDV เรื้อรัง รวมถึงผู้ที่มีภาวะตับแข็งระยะต้น (compensated cirrhosis)
เอกสารอ้างอิง
1. MIMS Thailand. Tobevibart–elebsiran combo demonstrates therapeutic potential against hepatitis D [internet]. 2025. [cited 2025 Dec 9]. Available from:
https://www.mims.com/thailand/news-updates/topic/tobevibart-elebsiran-combo-demonstrates-therapeutic-potential-against-hepatitis-d.
2. Asselah T, Chattergoon MA, Jucov A, et al. A phase 2 trial of tobevibart plus elebsiran in hepatitis D. N Engl J Med. Published online November 9, 2025. doi:10.1056/NEJMoa2508827.
3. World Health Organization. Hepatitis D [Internet]. Geneva: World Health Organization; 2023 [cited 2025 Dec 9]. Available from:
https://www.who.int/news-room/fact-sheets/detail/hepatitis-d.
4. Vir Biotechnology. Vir biotechnology presents positive chronic hepatitis delta clinical trial data and announces initiation of phase 3 registrational program [Internet]. News release. 2024 [cited 2025 Dec 15]. Available from:
https://investors.vir.bio/news/news-details/2024/Vir-Biotechnology-Presents-Positive-Chronic-Hepatitis-Delta-Clinical-Trial-Data-and-Announces-Initiation-of-Phase-3-Registrational-Program/default.aspx.

