|
อาจารย์ ภญ.วิภารักษ์ รัตนวิภานนท์ รองศาสตราจารย์ ดร.ภก.จิรพงศ์ สุขสิริวรพงศ์ ภาควิชาเภสชกรรม คณะเภสัชศาสตร์ มหาวิทยาลัยมหิดล |
|
| 66,575 ครั้ง เมื่อ 1 ช.ม.ที่แล้ว | |
| 2021-07-28 |
สถานการณ์การระบาดของ COVID-19 ยังคงสร้างความกังวลใจไปทั่วโลก และนับวันจะทวีความรุนแรงมากยิ่งขึ้น เชื้อไวรัส COVID-19 นี้เป็นไวรัสชนิดอาร์เอ็นเอ (RNA virus) ที่มีความสามารถในการกลายพันธุ์ได้ง่าย จึงกลายเป็นปัญหาที่สำคัญของการควบคุมโรค นอกจากการค้นคว้าหายาที่จะช่วยบรรเทาความรุนแรงของโรครวมถึงช่วยลดอัตราการเสียชีวิตของผู้ป่วยแล้ว การป้องกันการติดเชื้อ COVID-19 และการลดความรุนแรงของโรคผ่านการสร้างภูมิคุ้มกันด้วยการฉีดวัคซีนยังเป็นอีกกลไกสำคัญในการจัดการการระบาดของเชื้อไวรัส COVID-19 ปัจจุบันมีการพัฒนาวัคซีนสำหรับเชื้อไวรัส COVID-19 หลากหลายรูปแบบ ไม่ว่าจะเป็นวัคซีนที่พัฒนามาจากเชื้อตาย (inactivated vaccine) วัคซีนชนิดไวรัลเวคเตอร์ (viral vector vaccine) วัคซีนชนิดเอ็มอาร์เอ็นเอ (mRNA vaccine) และวัคซีนชนิดชิ้นส่วนโปรตีน (protein subunit vaccine) การพัฒนาวัคซีนด้วยวิธีการผลิตที่แตกต่างกันนี้ทำให้เกิดความแตกต่างในหลายด้าน บทความนี้จะกล่าวลงรายละเอียดเกี่ยวกับวัคซีนชนิด mRNA โดยเฉพาะประเด็นที่เกี่ยวข้องกับส่วนประกอบของวัคซีนรวมถึงข้อกังวลต่าง ๆ ที่เกี่ยวข้องกับวัคซีนชนิดนี้ 
ภาพจาก : https://www.news-medical.net/image.axd?picture=2021%2F6%2Fshutterstock_1907619673.jpg
mRNA vaccine กระตุ้นภูมิคุ้มกันต่อเชื้อ COVID-19 ได้อย่างไร?
mRNA เป็นสารพันธุกรรมชนิดหนึ่งในสิ่งมีชีวิตรวมถึงไวรัสด้วย แนวคิดของการพัฒนาวัคซีนด้วย mRNA คือ เมื่อนำส่งสารพันธุกรรมชนิดนี้เข้าสู่ร่างกายมนุษย์ ร่างกายจะมีการสร้างโปรตีนหนาม (spike protein) ซึ่งเป็นโปรตีนส่วนที่จะกระตุ้นให้ร่างกายเกิดการสร้างภูมิคุ้มกันต่อไวรัส COVID-19 ต่อไป อย่างไรก็ตาม สารพันธุกรรมนี้มีความคงตัวต่ำ เมื่อฉีดเข้าสู่ร่างกาย จะสลายตัวได้อย่างรวดเร็วโดยเอนไซม์ไรโบนิวคลีเอส (ribonucleases, RNase) และอาจไม่คงตัวในเซลล์เนื่องจากกลไกการปกป้องของเซลล์เจ้าบ้าน จึงไม่สามารถนำส่ง mRNA เข้าสู่ร่างกายโดยตรง นอกจากนี้ mRNA เกิดการเสื่อมสลายได้ทั้งทางกายภาพและทางเคมี จึงเป็นที่มาของการพัฒนาระบบนำส่งสารพันธุกรรมชนิด mRNA นั่นคือ การใช้อนุภาคนาโนชนิดไขมัน (lipid nanoparticles, LNP) ซึ่งวัคซีนสำหรับการติดเชื้อไวรัส COVID-19 ชนิด mRNA ที่มีการใช้ในปัจจุบันและรู้จักกันคือ Pfizer-BioNTech COVID-19 vaccine และ Moderna COVID-19 vaccine วัคซีนของทั้ง 2 บริษัทนี้ใช้ระบบอนุภาคนาโนชนิดไขมันเพื่อเพิ่มความคงตัวของ mRNA และสามารถนำส่ง mRNA เข้าสู่ร่างกายเพื่อกระตุ้นการสร้างภูมิคุ้มกันได้
เมื่อบริหาร mRNA COVID-19 vaccine เข้าสู่ร่างกายโดยการฉีดเข้ากล้ามเนื้อจะเกิดกระบวนการอักเสบแบบเฉพาะที่และเหนี่ยวนำให้เม็ดเลือดขาวนิวโทรฟิลและเซลล์ชนิด antigen presenting (APCs) มารวมกันบริเวณที่ฉีด จากนั้นเซลล์ชนิด APCs จะกลืนกินอนุภาคนาโนที่ห่อหุ้ม mRNA เข้าไป แล้วจึงเคลื่อนที่ไปยังระบบระบายน้ำเหลือง (draining lymph nodes) ซึ่งเป็นบริเวณที่มีเซลล์ในระบบภูมิคุ้มกันชนิด T (T cells) อยู่ จากนั้นจึงเกิดการกระตุ้นให้เกิดการสร้างภูมิคุ้มกันต่อเชื้อไวรัส COVID-19 จากกระบวนการดังกล่าว อนุภาคนาโนชนิดไขมัน (lipid nanoparticles) นี้เป็นส่วนสำคัญที่ทำให้เกิดการกระตุ้นระบบภูมิคุ้มกันของร่างกายโดยไม่ต้องอาศัยสารเสริมฤทธิ์ (adjuvant) อื่นเพิ่มเติม และอาจเป็นอีกปัจจัยหนึ่งที่ทำให้ mRNA vaccine กระตุ้นภูมิคุ้มกันขึ้นได้ค่อนข้างสูงเมื่อเปรียบเทียบกับวัคซีนชนิดอื่น ๆ
องค์ประกอบของ mRNA COVID-19 vaccine
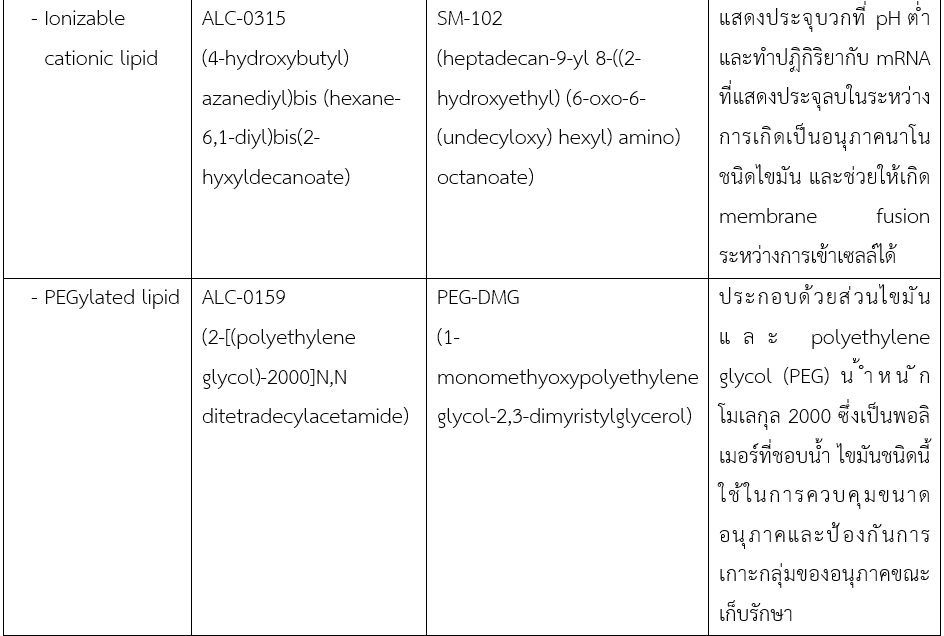
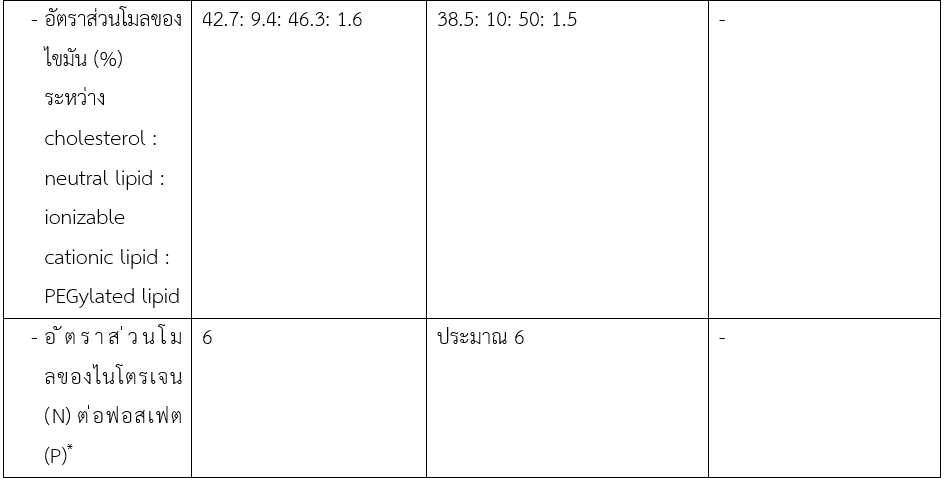
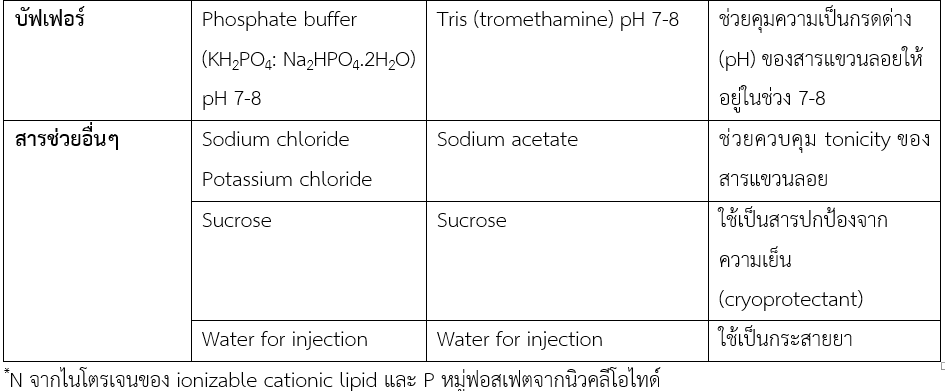
mRNA COVID-19 vaccine ของทั้ง 2 บริษัทนี้ มีส่วนประกอบหลัก 3 ส่วน ได้แก่ mRNA ซึ่งเป็นสารออกฤทธิ์ (active ingredient) ของวัคซีน อนุภาคนาโนชนิดไขมัน และสารช่วยอื่น ๆ อนุภาคนาโนชนิดไขมันนี้ มีองค์ประกอบหลัก 4 ส่วนได้แก่ คอเลสเตอรอล ไขมันชนิดประจุบวก (ionizable cationic lipid) ไขมันชนิดเป็นกลาง (neutral lipid) และ ไขมันชนิด PEGylated (PEGylated lipid) ซึ่งสารแต่ละชนิดมีหน้าที่ในตำรับที่แตกต่างกัน และสารที่ทั้ง 2 บริษัทนี้เลือกใช้ มีทั้งความเหมือนและความแตกต่างกันในรายละเอียด ดังแสดงไว้ในตารางที่ 1 จากองค์ประกอบเหล่านี้ ทำให้อนุภาคนาโนชนิดไขมันที่บรรจุ mRNA อยู่มีขนาดอนุภาคอยู่ในช่วง 60-100 นาโนเมตร 
ความคงตัวและการเก็บรักษา mRNA COVID-19 vaccine
จากข้อมูลความคงตัวของ mRNA และอนุภาคนาโนชนิดไขมัน พบว่า mRNA มีความไม่คงตัวมากกว่าอนุภาคนาโนชนิดไขมัน ในการเตรียมอนุภาคนาโนชนิดไขมันนี้ mRNA จะถูกห่อหุ้มไว้ด้านในอนุภาค และโมเลกุลของน้ำล้อมรอบโมเลกุลของ mRNA อยู่ภายในอนุภาคนาโนด้วย เนื่องจาก mRNA เป็นโมเลกุลที่ละลายในน้ำได้ดี อย่างไรก็ตาม น้ำที่ล้อมรอบ mRNA อาจเป็นสาเหตุหนึ่งที่ทำให้เกิดการเสื่อมสลายของ mRNA โดยปฏิกิริยา hydrolysis ได้หากเก็บที่อุณหภูมิสูงกว่าจุดเยือกแข็งของน้ำ ทำให้วัคซีนชนิดนี้ต้องเก็บในสภาวะที่ถูกแช่แข็งที่อุณหภูมิต่ำมากๆ ตลอดเวลาเพื่อเพิ่มความคงตัวของ mRNA ในระหว่างการเก็บรักษา การขนส่งหรือการกระจายวัคซีน และอายุของวัคซีนที่ค่อนข้างสั้น เมื่อเทียบกับวัคซีนชนิดอื่นๆ อย่างไรก็ตามความแตกต่างของอายุและอุณหภูมิที่ใช้ในการเก็บรักษาของวัคซีนทั้ง 2 บริษัทนี้ ยังไม่เป็นที่ทราบแน่ชัดว่าเกิดจากสาเหตุใด อาจต้องรอข้อมูลการศึกษาความคงตัวจากบริษัทที่อาจมีการเผยแพร่เพิ่มเติมในอนาคต นอกจากนี้ หากมีการศึกษาที่มากพอหรือมีการเปลี่ยนรูปแบบของวัคซีนให้อยู่ในรูปผงแห้งด้วยกระบวนการทำให้แห้งด้วยการแช่เยือกแข็ง (lyophilization) ก็อาจสามารถยืดอายุการเก็บรักษาของวัคซีนชนิดนี้ และอาจไม่จำเป็นต้องเก็บที่อุณหภูมิเยือกแข็งต่ำมาก ๆ ดังเช่นในปัจจุบัน
จากข้อมูลความคงตัวของวัคซีนทั้ง 2 บริษัท ที่มีการเปิดเผยออกสู่สาธารณะ ระบุความคงตัวและการเก็บรักษาสำหรับขวดวัคซีนที่ยังไม่ได้เปิดใช้ โดยสรุปดังนี้
-Pfizer-BioNTech COVID-19 vaccine
- สำหรับขวดวัคซีนที่แช่แข็ง เก็บที่อุณหภูมิ -90 ถึง -60 องศาเซลเซียส ได้เป็นเวลา 6 เดือน โดยในช่วงเวลาดังกล่าว สามารถเก็บและขนส่งที่อุณหภูมิ -25 ถึง -15 องศาเซลเซียส ได้เพียง 1 ครั้ง เป็นเวลา 2 สัปดาห์เท่านั้น และสามารถนำกลับไปแช่แข็งที่อุณหภูมิ -90 ถึง -60 องศาเซลเซียสได้
- สำหรับขวดวัคซีนที่ละลายน้ำแข็งแล้ว ที่อุณหภูมิ 2-8 องศาเซลเซียส มีอายุ 1 เดือน ที่อุณหภูมิ 2-8 องศาเซลเซียส
-- Moderna COVID-19 vaccine เก็บขวดวัคซีนในรูปสารแขวนลอยที่แช่แข็ง ที่อุณหภูมิ -25 ถึง -15 องศาเซลเซียส ได้เป็นเวลา 7 เดือน และเมื่อเก็บในตู้เย็นที่อุณหภูมิ 2-8 องศาเซลเซียสและป้องกันแสง วัคซีนมีอายุ 30 วัน
อย่างไรก็ตามเอกสารกำกับยาของวัคซีนทั้ง 2 บริษัท มีระบุรายละเอียดเกี่ยวกับวิธีการเก็บรักษา การเจือจาง การขนส่ง อายุของวัคซีนขณะเก็บรักษาที่อุณหภูมิต่างๆ อายุของวัคซีนขณะขนส่ง และอายุของวัคซีนหลังเจือจาง ไว้อย่างละเอียด ซึ่งสามารถอ่านเพิ่มเติมได้จากเอกสารกำกับยาของวัคซีนทั้ง 2 บริษัทได้
ข้อกังวลที่เกิดขึ้นเกี่ยวกับ mRNA COVID-19 vaccine
เนื่องจาก mRNA COVID-19 vaccine เป็นเทคโนโลยีการผลิตวัคซีนในรูปแบบที่ค่อนข้างใหม่ จึงมีข้อกังวลในหลากหลายประเด็น ดังนี้
-mRNA COVID-19 vaccine ทำให้เกิดการกลายพันธุ์ในมนุษย์ได้หรือไม่?
- จากข้อมูลในปัจจุบันพบว่า กลไกการออกฤทธิ์ของวัคซีนชนิดนี้ไม่มีการรบกวนการทำงานของนิวเคลียสซึ่งบรรจุดีเอ็นเอ (DNA) ที่เป็นสารพันธุกรรมหลักของมนุษย์ไว้ภายใน อย่างไรก็ตาม วัคซีนชนิดนี้ถือเป็นเทคโนโลยีใหม่ของการพัฒนาวัคซีน จึงยังไม่มีข้อมูลเกี่ยวกับผลข้างเคียงในระยะยาว
-mRNA COVID-19 vaccine มีอาการข้างเคียงอะไรบ้าง?
- อาการข้างเคียงที่พบบ่อยแต่มีความรุนแรงต่ำ คือ อาการข้างเคียงหลังฉีดวัคซีน เช่น เจ็บบริเวณที่ฉีด ไข้ หนาวสั่น ซึ่งส่วนใหญ่จะหายไปภายใน 2-3 วัน
- อาการข้างเคียงชนิดรุนแรงแต่พบได้น้อยมาก เช่น อาการแพ้แบบรุนแรง (anaphylaxis) ซึ่งพบได้ประมาณ 10 ราย จากการฉีดวัคซีน 1 ล้านโดส (ส่วนใหญ่เกิดภายใน 15 นาทีหลังฉีด ซึ่งอาจเกิดจากส่วนประกอบของไขมันชนิด PEGylated ที่มีรายงานว่าอาจก่อให้เกิดการแพ้ได้บ้าง รวมถึงอาจเกิดจากส่วนประกอบอื่น ๆ ของวัคซีน) รวมถึงมีรายงานการเกิดภาวะกล้ามเนื้อหัวใจอักเสบในประชากรเพศชายอายุน้อย ซึ่งส่วนใหญ่อาการไม่รุนแรง จากข้อมูลในปัจจุบันพบประมาณ 12-18 ราย จากการฉีดวัคซีน 1 ล้านโดส
-mRNA vaccine มีส่วนประกอบของแม่เหล็กหรือไม่?
- จากข้อมูลส่วนประกอบดังที่ระบุในเอกสารกำกับยาของวัคซีนทั้ง 2 บริษัทนี้ ไม่มีส่วนประกอบของสารที่มีคุณสมบัติเป็นแม่เหล็กอยู่ในวัคซีนดังที่มีการส่งต่อข้อมูลกันในสื่อออนไลน์
บทสรุป
โดยสรุป mRNA COVID-19 vaccine เป็นอีกหนึ่งความหวังของการลดความรุนแรงของการติดเชื้อ COVID-19 รวมถึงควบคุมการระบาดของโรค วัคซีนชนิดนี้ถือเป็นเทคโนโลยีใหม่ของการพัฒนาวัคซีน โดยใช้ความรู้ทางนาโนเทคโนโลยีเข้ามาเพิ่มประสิทธิภาพและความคงตัวของสารพันธุกรรมชนิด mRNA อย่างไรก็ตาม จากข้อมูลในปัจจุบันพบว่า วัคซีนชนิดนี้มีประสิทธิภาพรวมถึงมีความปลอดภัยค่อนข้างสูง เมื่อพิจารณาจากประโยชน์ที่จะได้รับและโทษที่อาจเกิดขึ้นแล้ว พบว่า ความคุ้มค่าของการสร้างภูมิคุ้มกันจากวัคซีนจึงมากกว่าความเสี่ยงที่จะเกิดจากผลข้างเคียง
แหล่งอ้างอิง/ที่มา
- Schoenmaker L, Witzigmann D, Kulkarni JA, Verbeke R, Kersten G, Jiskoot W, et al. mRNA-lipid nanoparticle COVID-19 vaccines: Structure and stability. International Journal of Pharmaceutics. 2021;601:120586.
- Moderna Biotech Spain, S.L. Summary of Product Characteristics for COVID-19 Vaccine Moderna. Revised: 06/2021. [Accessed 07/25/2021]. Available from: https://www.gov.uk/government/publications/regulatory-approval-of-covid-19-vaccine-moderna/information-for-healthcare-professionals-on-covid-19-vaccine-moderna
- EMA, 2020. Assessment report Comirnaty Common name: COVID-19 mRNA vaccine (nucleoside-modified). [Accessed 07/25/2021]. https://www.ema.europa.eu/en/documents/assessment-report/comirnaty-epar-public-assessment-report_en.pdf.
- Moderna US, Inc. Fact Sheet for Healthcare Providers Administering Vaccine: Moderna COVID-19 vaccine. Revised: 06/2021. [Accessed 07/25/2021]. Available from: https://www.fda.gov/media/144637/download.
- Pfizer Inc., BioNTech Manufacturing GmbH. Fact Sheet for Healthcare Providers Administering Vaccine: Pfizer-Biontech COVID-19 vaccine. Revised: 06/2021. [Accessed 07/25/2021]. Available from: https://www.fda.gov/media/144413/download.
- กรมควบคุมโรค, 2564. แนวทางการให้วัคซีนโควิด 19 ในสถานการณ์การระบาดปี 64 ของประเทศไทย กุมภาพันธ์ 2564. กรมควบคุมโรค กระทรวงสาธารณสุข [อินเตอร์เน็ต]. 2564. [เข้าถึงเมื่อ 25 กรกฎาคม 2564]. เข้าถึงได้จาก: https://ddc.moph.go.th/vaccine-covid19/getFiles/11/1620107083101.pdf
- Izda V, Jeffries MA, Savalha AH. COVID-19: A review of therapeutic strategies and vaccine candidates. Clin Immunol. 2021;222:108634.
- Centers for Disease Control and Prevention. COVID-19 mRNA vaccines in adolescents and young adults: Benefit-risk discussion [internet]. 2021. [cited 2021 July 26]. Available from: https://www.cdc.gov/vaccines/acip/meetings/downloads/slides-2021-06/05-COVID-Wallace-508.pdf
- Centers for Disease Control and Prevention. Allergic Reactions Including Anaphylaxis After Receipt of the First Dose of Pfizer-BioNTech COVID-19 Vaccine — United States, December 14–23, 2020 [internet]. 2021. [cited 2021 July 26]. Available from: https://www.cdc.gov/mmwr/volumes/70/wr/mm7002e1.htm
บทความที่ถูกอ่านล่าสุด

|
ข้อควรระวัง การใช้มาสคาร่า และการต่อขนตาให้ยาวและหนาขึ้น 5 วินาทีที่แล้ว |

|
ยาลดไขมันในเลือด : ตอนยาลดไตรกลีเซอไรด์ 9 วินาทีที่แล้ว |

|
เรื่องของยาลดความอ้วน orlistat 10 วินาทีที่แล้ว |

|
ดาหลา ความงามที่กินได้... 15 วินาทีที่แล้ว |

|
เมารถ เมาเรือ เมาเครื่องบิน ... รับมือได้อย่างไร 19 วินาทีที่แล้ว |
|
เมื่อสัตว์เลี้ยงได้รับสารพิษ : แนวทางการปฐมพยาบาลเบื้องต้น 20 วินาทีที่แล้ว |
|
ต้อลม-ต้อเนื้อ 25 วินาทีที่แล้ว |

|
บัวตอง ... ดอกไม้บนยอดดอย 30 วินาทีที่แล้ว |
|
เทคนิคป้อนยาสุนัขและแมวที่ไม่ยากอย่างที่คิด 34 วินาทีที่แล้ว |

|
วิตามินดี ป้องกันกระดูกหัก.....จริงหรือ 1 นาทีที่แล้ว |
