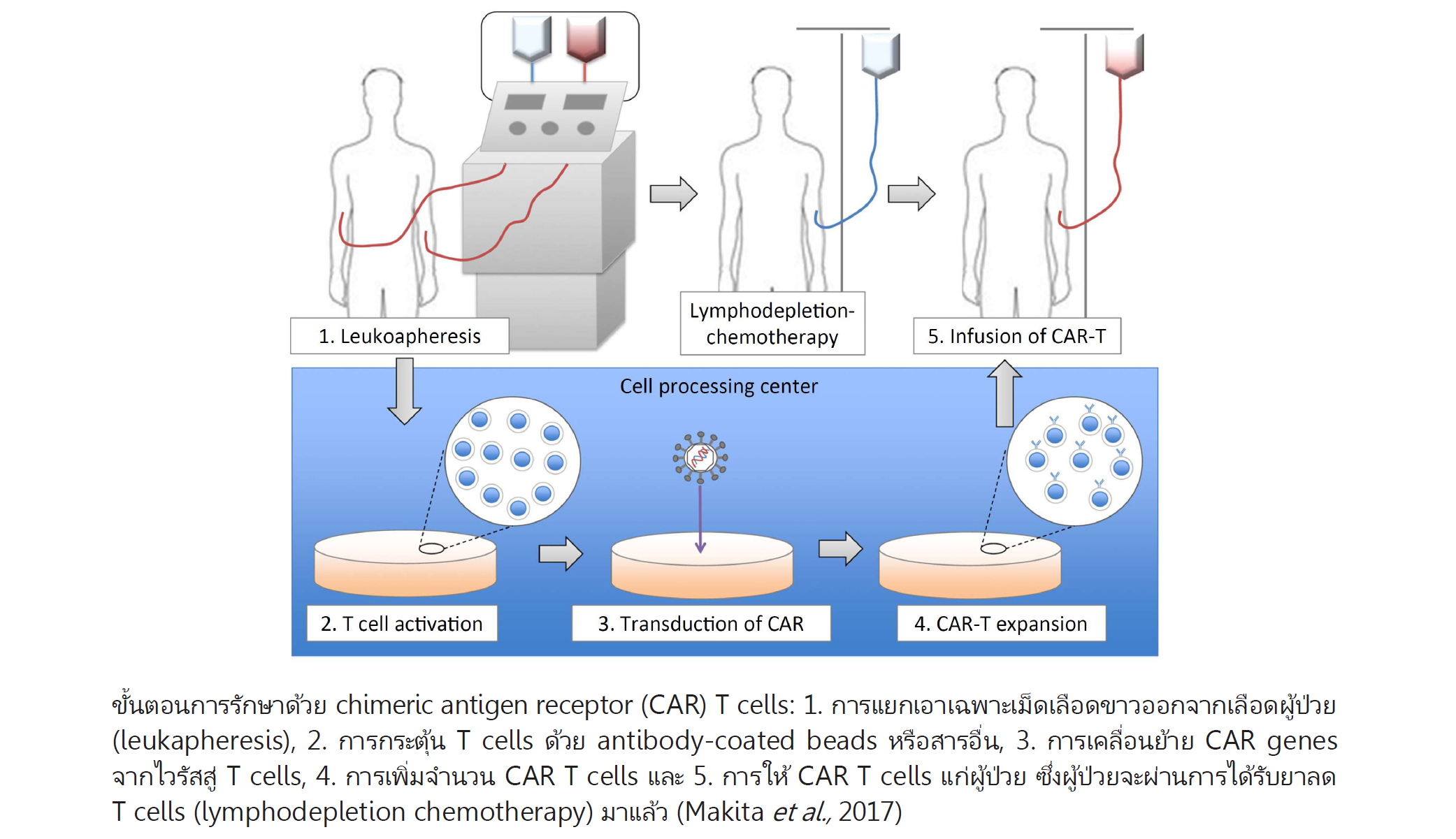
การรักษาโรคมะเร็งมีหลายวิธี มีทั้งการผ่าตัด การใช้เคมีบำบัด (chemotherapy) และการใช้รังสีรักษา (radiotherapy) เมื่อหลายปีมานี้ได้มีแนวคิดเกี่ยวกับการใช้ภูมิคุ้มกันบำบัด (immunotherapy) โดยการทำให้ระบบภูมิคุ้มกันของผู้ป่วยสามารถทำลายเซลล์มะเร็งได้ โดยอาศัยการทำงานของ T cells ซึ่ง T cells เป็นเม็ดเลือดขาวชนิดลิมโฟไซต์ มีตัวรับ (T cell receptor หรือ TCR) ที่สามารถจดจำและจับได้กับแอนติเจนที่จำเพาะ ดังนั้นหากมีการกระตุ้นให้ T cells มีการทำงานอย่างมีประสิทธิภาพและให้มีการแสดงออกของตัวรับที่มีความจำเพาะต่อเซลล์มะเร็งจะเกิดประโยชน์อย่างมาก ด้วยแนวคิดนี้ร่วมกับการใช้วิธีการ adoptive cell transfer (การนำ T cells จากผู้ป่วยมาเข้าสู่กรรมวิธีการผลิตให้มีประสิทธิภาพสูงจากนั้นนำกลับไปให้กับผู้ป่วย) ปัจจุบันได้นำมาใช้ผลิต T cells ที่มี TCR จับจำเพาะได้กับโปรตีน CD19 ซึ่ง CD19 เป็นโปรตีนที่พบได้มากบน B cells ที่เป็นมะเร็ง (แม้พบบน B cells ปกติได้ด้วย) โดยเริ่มจากการผลิต TCR ที่มีลักษณะเป็นโปรตีนลูกผสม (chimeric antigen receptor หรือ CAR) ซึ่งตรง extracellular CAR region มีส่วนที่เป็น antibody fragment ที่เจาะจงต่อโปรตีน CD19 จากนั้นนำ T cells ของผู้ป่วยเอง (autologous T cells) ที่แยกจากเลือดโดยวิธีการ leukapheresis (ดูรูป) หลังจากผ่านขั้นตอนการกระตุ้น T cells ด้วย antibody-coated beads (anti-CD3 หรือ anti-CD3/anti-CD28 beads) แล้ว จากนั้นด้วยวิธีการทางพันธุวิศวกรรม (genetic engineering) โดยอาศัยไวรัส (อาจใช้วิธีอื่นแต่ขณะนี้ประสิทธิภาพยังไม่ดีพอ) ช่วยในการใส่ CAR-encoding gene ให้ T cells เพื่อให้มีการแสดงออกของ CARs ที่เจาะจงต่อโปรตีน CD19 (CD19-CAR T cells) จากนั้นทำการเพิ่มจำนวน CD19-CAR T cells ให้เพียงพอเพื่อนำกลับไปใช้เป็นยาให้กับผู้ป่วย ซึ่งก่อนให้ CD19-CAR T cells นี้ผู้ป่วยต้องได้รับยาลด T cells ในร่างกาย (lymphodepletion chemotherapy) ป้องกันไม่ให้ร่างกายต่อต้านยาและช่วยเพิ่มประสิทธิภาพยา เมื่อ CD19-CAR T cells อยู่ในร่างกายจะทำหน้าที่เป็น “living drugs” ที่ฆ่าเซลล์มะเร็งที่มีโปรตีน CD-19 บนผิวเซลล์ อย่างไรก็ตาม การให้ CD19-CAR T cells จะทำอันตรายต่อเซลล์ปกติที่มีการแสดงออกของโปรตีน CD-19 ได้ด้วย อีกทั้งยังทำให้เกิด overproduction ของ inflammatory cytokines ด้วยเหตุนี้จึงเสี่ยงต่อการเกิดอาการไม่พึงประสงค์หลายอย่าง โดยเฉพาะอย่างยิ่งการเป็นพิษต่อระบบประสาท (neurological toxicities) และ cytokine release syndrome ซึ่งอาจเป็นอันตรายถึงชีวิตได้ ปัจจุบัน CD19-CAR T cells ที่ผลิตออกใช้แล้วได้แก่ tisagenlecleucel และ axicabtagene ciloleucel ชนิดแรกใช้รักษา acute lymphoblastic leukemia (ALL) ซึ่งเป็นมะเร็งเม็ดเลือดขาวที่มี CD19 บน B cells พบมากในเด็ก ส่วนชนิดหลังใช้รักษา B-cell non-Hodgkin lymphoma (B-NHL) ในผู้ใหญ่
อ้างอิงจาก
(1) Hay KA, Turtle CJ. Chimeric antigen receptor (CAR) T cells: lessons learned from targeting of CD19 in B cell malignancies. Drugs 2017;77: 237-45; (2) Makita S, Yoshimura K, Tobinai K. Clinical development of anti-CD19 chimeric antigen receptor T-cell therapy for B-cell non-Hodgkin lymphoma. Cancer Sci 2017;108:1109-18; (3) FDA approves first CAR T-cell therapy – the evolution of CAR T-cell therapy.
http://cellculturedish.com/2017/10/fda-approves-first-car-t-cell-therapy-evolution-car-t-cell-therapy/

