|
รองศาสตราจารย์แม้นสรวง วุฒิอุดมเลิศ ภาควิชาจุลชีววิทยา คณะเภสัชศาสตร์ มหาวิทยาลัยมหิดล |
|
| 44,425 ครั้ง เมื่อ 3 ช.ม.ที่แล้ว | |
| 2014-11-02 |
ในลำไส้ของสิ่งมีชีวิต เป็นแหล่งอาศัยของจุลินทรีย์หลายชนิดจำนวนมาก บางชนิดสร้างสารมีประโยชน์ต่อร่างกาย บางชนิดช่วยป้องกันการบุกรุกจู่โจมจากจุลินทรีย์ก่อโรค ตัวอย่างเช่น โยเกิร์ต ซึ่งเต็มไปด้วยจุลินทรีย์ชนิดดี ผู้บริโภคจึงมักศึกษาฉลากว่า ในถ้วยหรือขวดนั้นๆ มีจุลินทรีย์กี่ล้านตัว หมดอายุหรือยังเพราะเราต้องการกินจุลินทรีย์ตัวเป็นๆ
คำว่า Fecal Microbiota Transplantation (FMT) คือ “การปลูกถ่ายเชื้อจุลินทรีย์ในอุจจาระ” ซึ่งหมายถึงการนำอุจจาระของคนที่มีสุขภาพแข็งแรงมีเชื้อจุลินทรีย์ชนิดดีไปใส่ในลำไส้ของผู้ติดเชื้อในลำไส้
เชื้อ Clostridium difficile และการก่อโรค
Clostridium difficile เป็นแบคทีเรียรูปแท่งที่ไม่ต้องการออกซิเจนในการเจริญเติบโต สร้างสปอร์ พบได้ในลำไส้ใหญ่ของมนุษย์โดยไม่เป็นอันตรายทั้งนี้เพราะร่างกายมีจุลินทรีย์ประจำถิ่นที่เป็นเสมือนกลไกคอยควบคุมเชื้อตัวนี้ไว้ไม่ให้ก่อโรค บางคนจึงเป็นแค่พาหะของเชื้อนี้โดยไม่แสดงอาการผิดปรกติใดๆ แต่สามารถแพร่กระจายเชื้อไปสู่สิ่งแวดล้อม เมื่อคนที่มีสุขภาพอ่อนแอหรือมีโรคเรื้อรังบางอย่างเช่น ผู้สูงอายุ และผู้ป่วยรักษาตัวอยู่ในโรงพยาบาลที่มีการแพร่เชื้อนี้ ได้สัมผัสกับสิ่งปนเปื้อนของเชื้อเช่น จากการใช้โถส้วม การล้างมือที่ไม่พอเพียงหลังการขับถ่าย เชื้อจึงกระจายจากคนหนึ่งไปสู่สิ่งแวดล้อมและไปยังผู้คนรอบข้าง ทำให้ผู้ได้รับเชื้อมีอาการท้องเสียซึ่งมีความรุนแรงแตกต่างกัน พบว่าจำนวนผู้ป่วยโรคระบบทางเดินอาหารจาก Clostridium difficile-associated disease (CDAD) มีมากขึ้น และอาการรุนแรงมากขึ้น การใช้ยาปฏิชีวนะ เช่น clindamycin penicillin, cephalosporin, vancomycin และ metronidazole ทำให้จุลินทรีย์ชนิดดีบางชนิดลดลง เชื้อ C. difficile จึงเพิ่มจำนวนมากขึ้นและสร้างสารพิษออกมา ผู้ป่วยร้อยละ 15 ถึง 30 จะกลับมามีอาการอีกหลังหยุดยา อาการท้องเสียนี้สามารถหายได้เองเมื่อหยุดใช้ยาปฏิชีวนะ
อาการของการติดเชื้อนี้คือถ่ายบ่อย ถ่ายเป็นน้ำปนมูกเลือด ปวดท้อง คลื่นไส้ ไปจนถึงมีตะคริว ไข้สูง ลำไส้บวม ใน อาการท้องร่วงที่รุนแรงทำให้ผู้ป่วยสูญเสียน้ำ เกลือแร่ หรืออิเล็กโตรลัยต์จนถึงมีภาวะช็อคได้ บางรายเมื่อส่องกล้องพบการอักเสบ (รูปที่ 1) 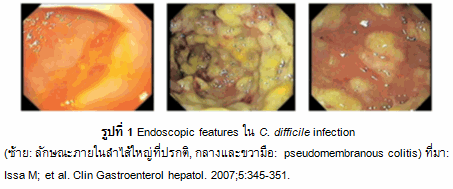
ที่มาของ FMT และผลการใช้
มีแนวคิดในการนำอุจจาระของผู้ที่มีสุขภาพแข็งแรง นำมาใส่ในลำไส้ใหญ่ของผู้ป่วยระหว่างการส่องกล้องตรวจลำไส้ (colonoscopy) ซึ่งการนำจุลินทรีย์ที่มีชีวิตจากอุจจาระคนหนึ่งเข้าสู่ลำไส้ใหญ่อีกคน เสมือนเป็นการเปลี่ยนถ่ายหรือการนำสิ่งมีชีวิตไปใส่ จึงเรียกว่า Fecal Transplantation ซึ่งเท่ากับเป็นการเพิ่มศักยภาพของจุลินทรีย์ประจำถิ่นชนิดดีที่เสียหายจากการใช้ยาปฏิชีวนะ ซึ่งจากผลการรักษาชี้ให้เห็นว่าการรักษาโดยวิธีนี้มีประสิทธิภาพและได้ผลดีกว่าการใช้ยาปฏิชีวนะ อย่างไรก็ตาม ผู้ป่วยที่ทรมานจากท้องร่วงเป็นๆหายๆ แม้จะส่งผลกระทบต่อสมรรถนะการดำเนินชีวิต แต่เมื่อได้รับการอธิบายกรรมวิธีจากแพทย์หรือผู้ให้การรักษา จะรู้สึกกระอักกระอ่วน หรือเกิดความสงสัยในผลที่อาจเกิดขึ้นจากการรักษาด้วยวิธีนี้
การรักษาด้วย FMT เป็นวิธีการที่ยังไม่มีเกณฑ์/ข้อบังคับเป็นสากล ดังนั้นการกำหนดรายละเอียดในวิธีการนำ FMT มาใช้จึงแตกต่างกัน เช่น ตัวอย่างจาก Amsterdam Protocol ระบุว่า อุจจาระที่นำมาใช้ต้องได้มาใหม่ ไม่เกิน 6 ชั่วโมง โดยใช้อย่างน้อย 150 กรัม ใส่ใน 0.9 % ของน้ำเกลือที่ฆ่าเชื้อแล้ว 500 มิลลิลิตร แล้วกรองให้ได้สารที่เป็นเนื้อเดียวกัน หรือบางแห่งกำหนดว่าผู้ให้อุจจาระ (stool donor) ต้องไม่ได้รับยาปฏิชีวนะภายใน 12 อาทิตย์ก่อนหน้า ไม่มีประวัติการผ่าตัดระบบทางเดินอาหาร และไม่มีการใช้ยากดภูมิคุ้มกัน เป็นต้น อย่างไรก็ตามขณะนี้ ได้มีการทดลองให้ frozen FMT capsule (รูปที่ 2) ในผู้ป่วย relapsing C. difficile infection 14 ราย ซึ่งประเมินประสิทธิภาพไว้เป็นด้านบวก และแนะนำการวิจัยกับผู้ป่วยจำนวนมากกว่านี้ 
อนาคตของ FMT ในมุมมองของ FDA
องค์การอาหารและยาของสหรัฐอเมริกา (FDA) ได้ลงความเห็นว่า FMT จัดเป็นทั้งยาและสารชีวภาพ เพื่อใช้กับคนไข้ที่ติดเชื้อ C. difficile infection ซ้ำอีกและรักษาด้วยวิธีมาตรฐานไม่ได้ผล มีการโฆษณาผลิตภัณฑ์และการรักษาโดยวิธีนี้ทางอินเตอร์เน็ตอย่างมากมาย โดยพยายามยกตัวอย่างบทความที่ระบุเฉพาะด้านดีเท่านั้นของการรักษาโดยวิธีนี้ แต่มีผู้วิจัยบางท่านเตือนว่าการใช้ FMT อย่างขาดความรับผิดชอบหรือไม่ระมัดระวัง อาจเป็นการเสี่ยงต่อการนำเชื้อก่อโรคอื่นให้แก่ผู้ป่วยได้ ด้วยเหตุนี้ FDA จึงได้จัดการประชุมเชิงปฏิบัติการใน ค.ศ. 2013 เพื่อแลกเปลี่ยนความคิดเห็นด้านวิทยาศาสตร์และจัดทำข้อกำหนดในการนำ FMT มาใช้และได้ออกเอกสารสำหรับภาคอุตสาหกรรม ในหัวข้อ 'Enforcement Policy Regarding IND (investigational new drug) Requirements for Use of Fecal Microbiota for Transplantation to Treat Clostridium difficile Infection Not Responsive to Standard Therapies' ด้วยแม้ว่ามีรายงานที่แสดงถึงผลดีของ FMT ในผู้ป่วยและมีผู้นำไปใช้อย่างแพร่หลาย แต่จะต้องประเมินประสิทธิผลและศึกษาความปลอดภัยจากกลุ่มตัวอย่างทดสอบด้านคลินิกโดยมีตัวควบคุมอย่างพอเพียง นอกจากนี้ ยังเปิดโอกาสให้ประชาชนที่สนใจแสดงข้อคิดเห็นได้ที่ องค์การอาหารและยาของสหรัฐอเมริกา
แหล่งอ้างอิง/ที่มา
- El-Matary W, Simpson R, Ricketts-Burns N. Fecal microbiota transplantation: are we opening a can of worms? Gastroenterology 2012;143:e19–e20.
- Gough E, Shaikh H, Manges AR. Systematic Review of Intestinal Microbiota Transplantation (Fecal Bacteriotherapy) for Recurrent Clostridium difficile Infection. Clin Infect Dis. 2011;53(10):994–1002.
- Kelly CP, Thomas LaMont J. Clostridium difficile — More Difficult Than Ever N Engl J Med 2008;359:1932-40.
- Kuijper EJ, Coignard B, T?ll P, ESCMID Study Group for Clostridium difficile, EU Member States; European Centre for Disease Prevention and Control: Emergence of Clostridium difficile-associated disease in North America and Europe. Clin Microbiol Infect 2006; 12 (Suppl 6):2–18.
- Leis S, Borody TJ, Jiang C, Campbell J. Fecal microbiota transplantation: A ‘How-To’ guide for nurses. Collegian 2014;280: 1-7.
- Matilla E, Uusitalo–Seppala R, Wuorelam M, Lehtola L, NurmiI H, Ristikankare M, Moilanen V, Salminen K, Seppala M, Matilla PS, Antilla V–J, Arkkila P. Fecal Transplantation, Through Colonoscopy, Is Effective Therapy for Recurrent Clostridium difficile Infection. Gastroenterol 2012;142:490–496.
- Meyer AM, Ramzan NN, Loftus EV Jr., Heigh RI, Leighton JA. The diagnostic yield of stool pathogen studies during relapses of inflammatory bowel disease. J Clin Gastroenterol 2004, 38:772-5.
- Shih C. The gut flora. J Lancaster Gen Hosp. 2013;8(4):114-147.
- Smits LP, BouterKEC, de vos WM, Borody TJ, Nieuwdorp M. Therapeutic Potential of Fecal Microbiota Transplantation Gastroenterol 2013;145:946–953.
- Tremaine WJ. Inflammatory Bowel Disease and Clostridium difficile–Associated Diarrhea: A Growing Problem. Clin Gastroent Hepatol 2007;5:310–311.
- van Nood E, Vrieze A, Nieuwdorp M, Fuentes S, Zoetendal EG, de Vos WM, Visser CE, Kuijper EJ, Bartelsman JF W.M, Tijssen JGP, Speelman P, Dijkgraaf MGW, Keller JJ. Duodenal Infusion of Donor Feces for Recurrent Clostridium difficile. N Engl J Med 2013;368:407-15.
- Youngster I, Russell GH, Pindar C, Ziv-Baran T, Sauk J, Hohmann EL. Oral, Capsulized, Frozen Fecal Microbiota Transplantation for Relapsing Clostridium difficile Infection. JAMA 2014: E1-E7.
บทความที่ถูกอ่านล่าสุด
|
โรคอุจจาระร่วงจากเชื้อ อีโคไล (E. coli) 3 วินาทีที่แล้ว |
|
หญ้าปักกิ่ง 12 วินาทีที่แล้ว |
|
กินยาพร้อมนม ได้ผลหรือไม่ ? 14 วินาทีที่แล้ว |

|
ยารักษาโรคเบาหวาน ใช้อย่างไร 1 นาทีที่แล้ว |

|
ผลิตภัณฑ์ถั่วเหลืองสำหรับสตรีวัยทอง (menopause) 1 นาทีที่แล้ว |

|
การปฐมพยาบาลด้วยสมุนไพร: สมุนไพรสำหรับอาการภายนอก 1 นาทีที่แล้ว |

|
หอมดอกปีบ 1 นาทีที่แล้ว |

|
สมุนไพรสู้ลมหนาว 1 นาทีที่แล้ว |

|
ปอบิด พิชิตสรรพโรคได้จริงหรือ? 1 นาทีที่แล้ว |

|
คะน้าเม็กซิโก…ต้นไม้แสนอร่อย 1 นาทีที่แล้ว |
